Резистентная артериальная гипертония
24.11.2005
Артериальная гипертония (АГ) определяется как резистентная (рефрактерная), если на фоне приема трех и более антигипертензивных препаратов различных классов (один из которых диуретик) в дозах, близких к максимальным, не удается достичь целевого артериального давления (АД) < 140/90 мм рт. ст. у большинства пациентов с АГ (или < 130/80 мм. рт. ст. у пациентов с сахарным диабетом и почечной недостаточностью).
По результатам исследования ALLHAT, было выявлено, что около 47% пациентов остались резистентными к антигипертензивной терапии спустя год после рандомизации, несмотря на жесткую схему титрации и комбинации препаратов, предусмотренную в данном исследовании. Сходные результаты (43% резистентных пациентов) были получены в Syst-Eur Study. По данным Yakovlevitch and Black, субоптимальный режим приема препаратов является наиболее частой причиной резистентности (43%), следующая по частоте причина — толерантность к лекарственным препаратам (22%), далее — вторичная АГ (11%), низкая комплаентность (10%).
Рефрактерная АГ (РАГ) может быть разделена на две большие категории: истинная РАГ и псевдорезистентная АГ.
ПСЕВДОРЕЗИСТЕНТНАЯ АГ
Проблемы, связанные с измерением АД
Основным правилам измерения АД, а также техническим факторам, влияющим на уровень АД, посвящено большое количество публикаций в медицинской печати и методических рекомендаций. Однако врачи общей практики зачастую пренебрегают существующими правилами измерения АД, что влечет за собой целый ряд ошибок:
- использование маленькой манжетки;
- измерение АД без предварительного отдыха;
- быстрое выпускание воздуха из манжетки:
- измерение АД на одной руке;
- аускультация до пальпаторного измерения АД.
Псевдогипертония диагностируется достаточно редко: в том случае, когда АД, измеренное по методу Короткова, не соответствует истинному (внутриартериальному) уровню АД. Этот феномен, связанный с выраженным атеросклерозом и кальцификацией плечевой и лучевой артерий, наблюдается у пожилых пациентов. Утолщение и уплотнение стенки артерий с возрастом приводит к тому, что для достижения компрессии ригидной артерии требуется более высокое давление (выше истинного) в манжетке, что приводит к завышению цифр АД. Наличие у пациента псевдогипертонии можно заподозрить при наличии следующих признаков:
- отсутствие поражений органов-мишеней;
- кальцификация плечевой и других артерий по данным исследований (рентген, УЗИ);
- АД в плечевой артерии выше, чем на ногах (что лишний раз иллюстрирует необходимость полного пропедевтического осмотра пациента);
- симптомы гипотензии на фоне антигипертензивной терапии при отсутствии выраженного снижения АГ (обычно трактуется у пожилых пациентов как усугубление неврологической симптоматики дисциркуляторной энцефалопатии в вертебро-базиллярном бассейне);
- тяжелая систолическая АГ.
Существование псевдогипертонии может быть верифицировано при наличии симптома Ослера — пальпация плечевой артерии даже когда внутриманжеточное давление превышает систолическое АД. Окончательное подтверждение диагноза возможно лишь при внутриартериальном измерении АД.
Низкая комплаентность
Комплаентность (приверженность пациентов к терапии) определяется как способность пациента точно следовать клиническим назначениям по приему лекарственных препаратов и модификации образа жизни. Прием лекарственных препаратов в соответствии с врачебными назначениями как минимум в 80% является наиболее общей характеристикой медикаментозной комплаентности. Низкая комплаентность встречается у более чем 50% пациентов, в том числе включенных в клинические исследования. Примечателен факт уменьшения количества пациентов с низкой приверженностью к терапии до 10% среди больных, наблюдающихся у специалистов по лечению АГ (США), что демонстрирует значение квалификации специалиста и дефицита временного фактора в общении с пациентом, который присутствует у врачей общей практики.
Многочисленные факторы, такие, как стоимость медикаментов, низкий интеллектуальный уровень пациента, сложности режима приема и дозирования и др., должны анализироваться врачом при диагностике РАГ и подозрении на низкую приверженность к терапии. Тщательный расспрос остается одним из наиболее оптимальных методов определения нарушений приверженности пациента к лечению. Врач должен устанавливать реалистичные краткосрочные цели для всех специфических компонентов лечения (контроль веса, снижение употребления соли, физическая активность, снижение употребления алкоголя и, по возможности, одно- либо двукратный режим дозирования препаратов) и максимально индивидуализировать свои рекомендации, исходя из конкретной клинической ситуации, социальных и семейных особенностей пациента.
Ошибки в назначении препаратов
Подобные ошибки представляют собой частую причину развития псевдорезистентной АГ. Несмотря на огромное количество клинических исследований, постоянную публикацию исследовательских и методических материалов в медицинской печати, широкое обсуждение правил назначения и комбинации препаратов среди врачей общей практики и кардиологов, ошибки в дозировании и комбинировании антигипертензивных препаратов встречаются достаточно часто.
Современная тактика медикаментозной гипотензивной терапии предусматривает возможность выбора между монотерапией и комбинированной терапией. Для получения целевых показателей АД у большинства пациентов, особенно с I–III степенью повышения АД, требуется назначение комбинированной терапии.
Среди преимуществ комбинированной антигипертензивной терапии можно выделить следующие:
- использование препаратов с различными механизмами действия позволяет контролировать несколько патогенетических звеньев АГ;
- входящие в комбинацию препараты используются в более низких дозах, что снижает вероятность развития побочных эффектов;
- при назначении фиксированных комбинаций (два препарата в одной таблетке) улучшается приверженность к терапии.
Эффективными и хорошо переносимыми считаются следующие лекарственные комбинации:
- диуретики и β-блокаторы (атенолол, бисопролол);
- диуретики и ингибиторы АПФ (каптоприл, лизиноприл, эналаприл) или антагонисты рецепторов к ангиотензину II (валсартан, лозартан);
- антагонисты кальция (дигидропиридины: амлодипин, нифедипин) и β-блокаторы;
- антагонисты кальция и ингибиторы АПФ или антагонисты рецепторов к ангиотензину II;
- антагонисты кальция и диуретики;
- α-блокаторы (доксазозин, теразозин) и β-блокаторы.
Могут использоваться и другие комбинации с препаратами центрального действия (α2-агонисты, агонисты имидазолиновых I2-рецепторов), а также трех- и более компонентная схема.
Рекомендуется использование длительно действующих препаратов, обеспечивающих эффект в течение 24 ч и требующих однократного приема в течение суток, что значительно улучшает приверженность к терапии.
Под неадекватным режимом использования препаратов подразумевается назначение гипотензивных препаратов в низких дозах, использование патогенетически неграмотных комбинаций (препараты одного класса, например верапамил и дигидропиридин, или препараты со сходным механизмом действия — ингибитор АПФ и антагонист рецепторов к ангиотензину II — или сходными побочными эффектами).
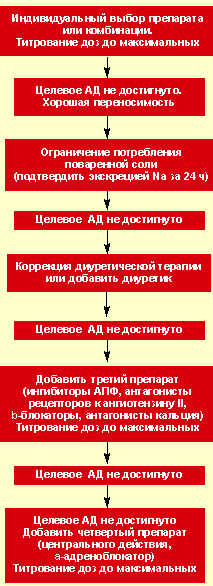
Алгоритм оптимизации антигипертензивной терапии приведен на рисунке 1.
|
| Рисунок 1. Алгоритм оптимизации лекарственной терапии |
Таким образом, в случае резистентной АГ клиницист должен тщательно проанализировать назначенную схему антигипертензивной терапии: убедиться в адекватности назначенных доз и патогенетической оправданности применяемых комбинаций, а также в правильности назначенного режима терапии (соотнесение длительности действия и кратности назначения препаратов). При необходимости следует добавить к используемой схеме еще один препарат, учитывая при этом индивидуальные особенности пациента (поражение органов-мишеней, ассоциированную и сопутствующую патологию).
ИСТИННАЯ РЕЗИСТЕНТНАЯ АГ
Повышенная вариабельность и реактивность АД
Гипертония «белого халата» («офисная гипертония», «кабинетная гипертония») определяется как состояние стабильного повышения АД во время измерения на приеме у врача при нормальных значениях вне лечебного учреждения. Рассматривается как проявление стресс-индуцированной гипертонии. По данным Brown и соавторов, 2–3 из каждых 10 пациентов с резистентной АГ при суточном мониторировании АД имеют хороший контроль АД (среднее значение менее 135/85 мм рт. ст.). Пациенты с данным феноменом часто демонстрируют повышенную чувствительность к антигипертензивным препаратам, которые значительно снижают «нестрессорное» АД и могут вызывать симптомы гипотензии. Пациенты в этом случае самостоятельно отменяют гипотензивные препараты или начинают принимать их хаотично, что значительно затрудняет ведение этих пациентов, снижает комплаентность.
В данном случае рекомендуется проведение внеофисного измерения АД (суточное мониторирование и дневники самоконтроля АД) до коррекции схемы антигипертензивной терапии. Несмотря на достаточную простоту диагностики данного феномена, клиницисты часто недооценивают его распространенность и значимость, что приводит к ошибкам в подборе схем лекарственной терапии и снижению комплаентности.
Барорефлекторная недостаточность
Нестабильность АД с периодами значительного повышения и снижения встречается у пациентов с повреждением барорефлекторной функции. Данное состояние встречается достаточно редко и очень трудно диагностируется.
Физиологическая резистентность (перегрузка объемом)
Наиболее частой причиной физиологической резистентности АГ является перегрузка объемом. Чрезмерное употребление соли может служить причиной развития РАГ у леченых пациентов. Использование прямых вазодилататоров (миноксидил, гидралазин), адреноблокирующих препаратов (α-блокаторы и β-блокаторы) и больших доз сильнодействующих диуретиков может приводить к увеличению задержки жидкости и формированию РАГ. Наиболее частой причиной персистирующей гиперволемии является назначение ежедневного однократного приема фуросемида. За снижением внутрисосудистого объема в течение нескольких часов после приема фуросемида следует активация ренин-ангиотензин-альдостероновой системы (РААС) с включением механизмов задержки натрия, которые восстанавливают весь потерянный натрий во время краткого интервала натрийуреза. При сохраненной функции почек назначение утренней дозы длительно действующего гидрохлортиазида (12,5–25 мг) способно разорвать этот порочный круг. Все препараты, снижающие АД, снижают также почечное перфузионное давление и клубочковую фильтрацию, что приводит к задержке натрия и жидкости.
К сожалению, многим пациентам с РАГ, которые получают несколько гипотензивных препаратов, не назначаются диуретики в адекватных дозах. Ограничение употребления соли само по себе приводит к адекватному контролю объема циркулирующей плазмы, снижению АД, улучшению переносимости лечения, уменьшению количества применяемых антигипертензивных препаратов. На фоне снижения употребления соли эффективность всех антигипертензивных препаратов повышается, за исключением антагонистов кальция.
При подозрении на перегрузку объемом необходимо определение количества натрия в суточной моче. При этом часто обнаруживается неадекватность в выполнении диетических рекомендаций у пациентов, которые утверждают, что соблюдают низкосолевую диету. У больных, не соблюдающих низкосолевую диету, экскреция натрия увеличивается.
Лекарственные взаимодействия
Идентификация лекарственных препаратов, снижающих эффективность антигипертензивной терапии, крайне важна, так как помогает индивидуально оптимизировать терапию у пациентов с учетом механизма действия применяемых препаратов. Остановимся лишь на наиболее часто применяемых.
Стероиды. АГ регистрируются у более чем 20% пациентов, принимающих синтетические кортикостероиды. Прием данных препаратов также может быть причиной резистентности АГ. Фактором риска развития РАГ является пожилой возраст. Такие лекарственные субстанции, как натуральная лакрица, фенилбутазон, карбеноксолон, препараты преднизолона, кортизола обладают минералокортикоидной активностью. Прием этих препаратов в средних дозах может приводить к псевдогиперальдостеронизму (задержка натрия, гиперволемия, гипокалиемия с метаболическим алкалозом и подавление плазменного ренина и альдостерона). Мази, антигеморроидальные препараты, глазные капли, ингаляционные бронходилататоры, назальные антиаллергические спреи могут содержать субстанции со значительной минералокортикоидной активностью. Некоторые из этих препаратов могут содержать симпатические амины. Для снижения АД и преодоления рефрактерности необходим отказ от применения этих препаратов. В случаях, когда терапия стероидами является обязательной, эффективными препаратами являются диуретики. В процессе терапии диуретиками необходим мониторинг калия, так как данные препараты способны усиливать гипокалиемию при стероидзависимой АГ.
Половые гормоны. Пероральные контрацептивы способны индуцировать АГ приблизительно в 5% случаев при использовании высокодозовых комбинаций эстрогенов и прогестинов. Фактором риска возникновения и усугубления АГ являются курение, ожирение, раса (афроамериканцы), диабет, почечная патология. Описаны случаи развития злокачественной АГ на фоне приема оральных контрацептивов. Следующей группой риска возникновения РАГ являются мужчины, принимающие эстрогены с целью лечения рака предстательной железы. Даназол, полусинтетический андроген, используемый для лечения эндометриоза, наследственного ангионевротического отека, может приводить к гиперволемии и усугублению АГ.
Препараты, влияющие на симпатическую нервную систему. Фенилэфрин, назначаемый в виде глазных капель, адреналоподобные вещества, используемые топически при глаукоме, могут приводить к росту АД у нормотоников и пациентов с АГ. Присоединение к антигипертензивной схеме α-блокаторов, α- и β-блокаторов нивелирует данные эффекты.
Большинство аноректиков, нежелательных для применения, состоят из комбинации антигистаминоподобных веществ и адренергических агонистов (обычно фенилпропаноламин, эфедрин, псевдоэфедрин или кофеин). α-адренергическая интоксикация, индуцированная назальными и пероральными деконгестантами и противокашлевыми препаратами, содержащими большие дозы оксиметазолина, фенилэфрина, эфедрина, может индуцировать АГ или усугублять уже имеющуюся патологию. Препараты выбора — α-блокаторы, α- и β-блокаторы.
Нестероидные противовоспалительные препараты. НПВС могут потенцировать повышение АД и конкурировать с антигипертензивными препаратами. НПВС повышают на 40% риск развития АГ. НПВС взаимодействуют с некоторыми антигипертензивными препаратами, такими, как диуретики, β-блокаторы, ингибиторы АПФ, но не с антагонистами кальция — препаратами центрального действия, антигипертензивная эффективность которых не связана с продукцией простагландинов. Индометацин, пироксикам, напроксен вызывают значительное повышение АД, тогда как сулиндак и полные дозы аспирина оказывают наименьшее воздействие на уровень АД. Минимальные дозы аспирина не влияют на показатели АД у пациентов с АГ. Селективные препараты-ингибиторы циклооксигеназы-2 (целекоксиб, рофекоксиб) не приводят к повышению АД и не оказывают дозозависимых эффектов на АД. Метаанализы показали, что НПВС приводят к увеличению среднего АД на 4–5 мм рт. ст. Они являются причиной задержки натрия, повышения чувствительности к прессорным гормонам. Принимая во внимание широкую распространенность заболеваний суставов и позвоночника среди пожилых пациентов, клиницисты должны отчетливо осознавать возможные взаимодействия НПВС с антигипертензивными препаратами.
Трициклические антидепрессанты. Трициклические антидепрессанты препятствуют гипотензивным эффектам адреноблокаторов, таких, как гуанетидин, что может приводить к значительному повышению АД. Эти препараты предупреждают накопление антигипертензивных препаратов в адренергических нервных окончаниях, где они блокируют передачу нервного возбуждения. Подобные взаимодействия описаны и для других гипотензивных препаратов (метилдопа, клонидин).
Ассоциированные состояния
Метаболический синдром и ожирение. Распространенность метаболического синдрома в настоящее время приобретает характер эпидемии и в некоторых странах, в том числе и России, достигает 25–35% среди взрослого населения.
У пациентов с метаболическим синдромом эффективность антигипертензивных препаратов снижается, и двухкомпонентная схема, как правило, не позволяет достичь целевого АД. Это связано с патогенетическими особенностями АГ при метаболическом синдроме.
В норме инсулин обладает сосудистыми протективными эффектами и вызывает инсулинобусловленную вазодилатацию. Но при хронической гиперинсулинемии и инсулинорезистентности запускаются другие патофизиологические механизмы, приводящие к АГ: стимуляция симпатико-адреналовой системы (САС), РААС; повышение содержания внутриклеточного Na+ и Са2+, уменьшение К+ с увеличением чувствительности сосудистой стенки к прессорным воздействиям; повышение реабсорбции Na+ в проксимальных и дистальных канальцах нефрона (задержка жидкости с развитием гиперволемии). Особое значение приобретает стимуляция пролиферации гладкомышечных клеток сосудистой стенки под действием гиперинсулинемии (сужение артериол и увеличение сосудистого сопротивления).
Неудачи в лечении АГ при метаболическом синдроме обусловлены, как правило, фокусировкой терапевтической тактики только на АГ. В основе успешной терапии лежит принцип одновременной коррекции всех звеньев патогенеза метаболического синдрома, всестороннее воздействие на причины и следствия инсулинорезистентности: изменение образа жизни, лечение ожирения, терапия нарушений углеводного обмена, лечение дислипидемии. При подборе антигипертензивной терапии следует учитывать следующие особенности: метаболические эффекты гипотензивных препаратов (влияние на липидный спектр, инсулинорезистентность, уровень глюкозы и мочевой кислоты); необходимость более частого использования 3-, 4-компонентной схемы терапии с воздействием на различные звенья патогенеза АГ, характерные для метаболического синдрома.
Курение приводит к транзиторному повышению АД, увеличению вариабельности АД. При большом количестве выкуриваемых сигарет продолжительность эпизодов гипертонии растет. Антигипертензивная эффективность β-адреноблокаторов у курящих больных АГ снижается.
Алкоголь. Злоупотребление алкоголем (хроническая алкогольная интоксикация) приводит к повышению АД у нормотоников и индуцированию резистентности к антигипертензивным препаратам. Существуют дозозависимые гипертензивные эффекты алкоголя. Основным видом лечения является прекращение или уменьшение употребления спиртных напитков. В некоторых случаях прекращение приема алкоголя не улучшает контроля АД.
Генетические особенности
Полигенный синдром эссенциальной гипертонии включает широкий спектр гемодинамических и нейроэндокринных особенностей. Так, плазменная активность ренина частично определяет индивидуальную чувствительность к β-блокаторам, ингибиторам АПФ, антагонистам рецепторов к ангиотензину II. Широко известна связь изменений гена ангиотензиногена с сольчувствительностью. Описаны генетически детерминированные изменения в метаболизме лекарственных препаратов, такие, как ускоренный метаболизм (гидралазин), но для основных классов гипотензивных препаратов значимые генетические особенности метаболизма не подтверждены. Общепризнана высокая чувствительность к диуретикам и относительно низкая к ингибиторам АПФ, β-блокаторам, антагонистам рецепторов к ангиотензину II у пациентов негроидной расы.
Вторичные формы АГ
Прогрессирование почечной недостаточности представляет собой наиболее частую и легко диагностируемую причину резистентности АГ. Реноваскулярные болезни широко распространены среди пациентов с ранее контролируемой АГ, особенно если атеросклеротические поражения присутствовали в других сосудистых бассейнах. В течение последних лет представление о влиянии первичного гиперальдостеронизма (ПГА) на распространенность РАГ серьезно изменилось. Исследователи отмечают большую частоту ПГА. Многие эти пациенты имеют нормальный уровень калия в плазме при повышенном уровне альдостерона плазмы относительно ренина. У большинства из них диагностируется билатеральная гиперплазия коры надпочечников, при которой не показано оперативное лечение. Препаратом выбора в данном случае является спиронолактон.
Синдром обструктивного апноэ сна (СОАС). По данным H. Issakson и соавторов, среди пациентов с рефрактерной в 56% случаев выявляется СОАС.
Обусловленная СОАС типичная «утренняя» АГ, преимущественно диастолическая, плохо поддается коррекции обычными гипотензивными препаратами. Клиницисты часто недооценивают значение этого состояния и не включают в традиционную схему сбора анамнеза вопросы, касающиеся храпа пациента, наличия остановок дыхания во сне. А это необходимо особенно у пациентов с ожирением.
Существуют достаточно противоречивые данные относительно эффективности и безопасности антигипертензивных препаратов различных групп у больных с СОАС. Так, выявляется ряд побочных эффектов при лечении некоторыми антигипертензивными препаратами, в частности угнетение тонуса мышц верхних дыхательных путей при лечении β-адреноблокаторами, α-метилдопой, а также в результате метаболического алкалоза, вызванного диуретиками. В других работах подтверждаются положительные эффекты диуретиков в виде уменьшения количества эпизодов дыхательных нарушений во время сна. Однозначно положительные данные получены при использовании антагонистов кальция и ингибиторов АПФ.
Однако для успешной терапии АГ при СОАС необходимо проведение комплекса лечебных мероприятий, направленных на устранение СОАС. Наиболее эффективными в настоящее время являются увулопалатофарингопластика, СРАР-терапия (постоянное положительное давление в дыхательных путях).
Алгоритм диагностики РАГ представлен на рисунке 2.
Необходимо помнить, что причиной резистентности АГ может быть сочетание нескольких экзогенных факторов и также вторичных форм АГ. Лечение РАГ предполагает элиминацию экзогенных факторов и использование максимально переносимых доз препаратов в многокомпонентной схеме терапии, включающей длительнодействующие диуретики. Многие исследования доказывают необходимость и целесообразность присоединения спиронолактона к 3- или 4-компонентной схеме терапии у пациентов с РАГ.
Литература
- Oparil S., Michael A. Weber. Hypertension: A Companion to Brenner and Rector’s The Kidney, 2000.
- Erdine S. Resistant hypertension. ESH. Scientific Newsletter, 2003; 4: N15.
- Hypertension Primer, Third Edition, 2003 American Heart Association.
- Европейские рекомендации по диагностике и лечению артериальной гипертонии, 2003.
Т. В. Адашева, кандидат медицинских наук, доцент
МГМСУ, Москва
Врезки:
