Лечащий Врач #3, 2008
Возможно ли поддержание строгого контроля углеводного обмена у больных сахарным диабетом на протяжении длительного времени?
Сахарный диабет (СД) продолжает оставаться тяжелым бременем для национальных служб здравоохранения всех стран мира. Он является одной из основных причин ранней инвалидизации и высокой летальности. Несмотря на принятие в большинстве стран мира национальных программ по борьбе с СД, его распространенность и заболеваемость продолжают увеличиваться не только среди населения старше 40 лет, но и среди подростков и лиц детского возраста [1]. Так, по данным Международной федерации диабета и ВОЗ в настоящее время во всем мире насчитывается более 200 млн больных диабетом. Экспертная оценка, проведенная авторитетными диабетологами мира, позволяет предполагать, что к 2010 г. в мире будет насчитываться более 239,4 млн, а к 2030 г. — около 380 млн больных СД, из которых более 90% будет приходиться на больных сахарным диабетом типа 2. Практически аналогичная ситуация по распространенности и заболеваемости сахарным диабетом наблюдается и в Российской Федерации: по сравнению с данными 1994 г. (8 млн), к 2010 г. число заболевших предполагаемо вырастет и составит 13 млн (Ю. И. Сунцов, 2007).
На самом деле эти данные могут оказаться заниженными, так как около 50% больных СД остаются недиагностированными, а следовательно, не получающими никакой сахароснижающей терапии и сохраняющими стабильную гипергликемию — все это создает благоприятные условия для развития сосудистых осложнений СД [2], из которых первоочередная роль в механизмах инициации и прогрессирования заболевания принадлежит хронической гипергликемии или отсутствию компенсации углеводного обмена у больных СД. Это было убедительно подтверждено исследованиями Американской диабетической ассоциации (АДА), результаты которых были доложены в 1993 г. на 53-м съезде этой ассоциации в Лас-Вегасе. Это исследование, известное в литературе как DCCT или «Контроль диабета и оценка его осложнений», проводилось в течение 10 лет и было посвящено изучению развития и скорости прогрессирования сосудистых осложнений у больных СД типа 1 в зависимости от степени компенсации диабета. Оно показало, что строгая компенсация заболевания позволяет осуществлять первичную профилактику ретинопатии на 76%; вторичную профилактику ретинопатии на 54%; клиническую нейропатию на 60%; исчезновение микроальбуминурии — на 39% и альбуминурии — на 54% [3]. С помощью других исследований [4, 5] было подтверждено, что нарушение углеводного обмена и наличие длительной гипергликемии является таким же фактором инициации и прогрессирования развития сосудистых осложнений и у больных, страдающих СД типа 2.
C учетом новых данных о взаимоотношениях между состоянием компенсации углеводного обмена и частотой сосудистых осложнений СД были пересмотрены критерии компенсации углеводного обмена у больных СД (табл. 1).
Из данных, представленных в таблице, видно, что практически все национальные диабетические ассоциации, ВОЗ и Всемирная федерация диабета (ВФД) рекомендуют поддерживать «строгую» компенсацию углеводного обмена, при которой уровень гликозилированного гемоглобина (HbA1c) в крови составлял бы < 7% или ≤ 6,5% или даже ниже 6,5% (при норме 6,0%). В консенсусе, разработанном в 2006 г. АДА и ВФД, подчеркивается, что показатель HbA1c > 7,0% следует рассматривать как недостаточную компенсацию углеводного обмена у больного СД типа 2 и как необходимость принятия конкретных действий по улучшению лечения для достижения снижения этого показателя до < 7,0% [11].
Такие «жесткие» рекомендации по контролю углеводного обмена являются следствием проведенного проспективного исследования UKPDS, результаты которого четко свидетельствуют о том, что при уменьшении уровня HbA1c на 1% общая летальность при СД типа 2 снижается на 21%, риск развития микрососудистых осложнений — на 37%, а инфаркта миокарда — на 14% [12].
Адекватность терапии СД остается самым актуальным вопросом, так как установлено, что гипергликемия является пусковым моментом многих патогенетических механизмов, способствующих развитию сосудистых осложнений. Поддержание «строгой» компенсации диабета, т. е. сохранение нормальной (или близко к нормальной) концентрации глюкозы в крови в течение длительного времени, является условием, при котором удается задержать или отсрочить время появления поздних осложнений СД и осуществлять первичную профилактику сосудистых осложнений диабета.
Помимо этого обязательным условием и целью проводимой терапии является мониторирование артериального давления (АД) и поддержание показателей АД в пределах < 130/80 мм рт. ст.
Лечение СД является комплексным и включает следующие компоненты:
-
диету;
-
дозированную физическую нагрузку;
-
обучение больного, самоконтроль состояния углеводного обмена и психологическую адаптацию к заболеванию;
-
применение сахароснижающих лекарственных средств;
-
профилактику и лечение поздних осложнений СД.
Необходимо подчеркнуть, что эффективное лечение СД и предупреждение или профилактика его сосудистых осложнений может быть достигнута лишь при условии обязательного выполнения всех компонентов проводимой терапии. Поэтому, как и прежде, основной задачей лечения СД является достижение его компенсации на протяжении длительного времени, что сопряжено с большими трудностями. Это связано с тем, что лечение СД обычно назначается не с момента нарушения углеводного обмена, выявляемого только с помощью проведения различных нагрузочных тестов (пробный завтрак, глюкозотолерантный тест и др.), а лишь при появлении выраженных клинических признаков диабета, свидетельствующих о развитии сосудистых и других изменений в тканях и органах. Поэтому профилактика поздних сосудистых осложнений диабета непосредственно зависит от ранней диагностики заболевания и компенсации углеводного обмена у больных СД на протяжении длительного времени.
Контроль за адекватностью лечения и сохранением указанных выше критериев компенсации углеводного обмена осуществляется с помощью применения глюкометров (кратковременный контроль гликемии) и определением содержания гликозилированного гемоглобина в крови (объективный показатель контроля гликемии на протяжении длительного времени).
Для определения содержания глюкозы в крови используются глюкометры производства различных фирм. Перечень наиболее часто применяемых в настоящее время глюкометров представлен в табл. 2.
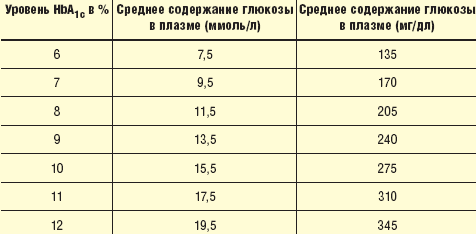
Содержание глюкозы в крови является объективным показателем компенсации углеводного обмена, но, к сожалению, лишь на определенный короткий отрезок времени. Показателем компенсации углеводного обмена на протяжении длительного времени (2 и более месяцев) является уровень гликозилированного гемоглобина в крови. Корреляция между этими показателями представлена в табл. 3.
Определение гликозилированного гемоглобина в крови является рутинным исследованием, и его уровень должен определяться не только при манифестации СД, как подтверждение наличия нарушенного углеводного обмена, но и как мониторинг компенсации заболевания на протяжении длительного времени.
Установлено, что в гемолизатах крови человека наряду с основной фракцией гемоглобина (HbA) содержится незначительное количество других фракций, названных «минорными» (НbА1а, А1b, A1c). У здоровых взрослых на долю НbА приходится 90%, НbА1а — 1,6%; НbА1в — 0,8%, НbА1с — 3,6%; НbА2 — 2,5% и НbF — 0,5%. Гликозилированный гемоглобин — это гемоглобин, в котором молекула глюкозы конденсируется с β-концевым валином в β-цепи молекулы НbА. Этот неферментативный процесс протекает медленно, в течение всей жизни эритроцита (около 120 дней). Установлено, что гликозилирование осуществляется через стадию образования альдимина («шиффовы основания» между альдегидом углеводов и аминогруппой), сравнительно нестойкого, «обратимого» соединения. Далее альдимин посредством химического преобразования (преобразование Амадори) превращается в относительно стойкое, «необратимое» соединение кетоамин. Образовавшийся кетоамин остается присоединенным к белку на весь период его жизни. Гликозилированию подвергаются многие белки организма (белки крови, хрусталика, почек, нервов, сосудов и др.). Скорость гликозилирования и количество гликозилированных белков зависит от величины и длительности гипергликемии.
НbА1с составляет 4–6% общего гемоглобина в крови практически здоровых лиц, тогда как у больных сахарным диабетом уровень этого белка повышен в 2–3 раза. Cодержание гликозилированного гемоглобина имеет прямую корреляцию с уровнем глюкозы в крови и является интегрированным показателем компенсации углеводного обмена на протяжении последних 60–90 дней. Скорость образования НbА1с, также как и НbА1, зависит от величины гипергликемии, а нормализация его уровня в крови происходит через 4–6 недель после достижения эугликемии. В связи с этим содержание гликогемоглобина является адекватным показателем компенсации углеводного обмена у больных диабетом на протяжении длительного времени. По рекомендации ВОЗ определение содержания гликозилированного гемоглобина в крови больных СД следует проводить 1 раз в квартал. Этот показатель широко используется как для скрининга населения и беременных женщин для выявления нарушения углеводного обмена, так и для контроля лечения больных СД.
Для определения содержания гликозилированного гемоглобина в крови предложено значительное количество различного оборудования. По решению Международной комиссии по лабораторному диагностическому оборудованию референс-оборудованием для определения гликозилированного гемоглобина является оборудование фирмы «Био-Рад».
Исследования, проведенные нами по определению содержания гликозилированного гемоглобина в крови различными методами, показали, что наиболее чувствительным, специфическим и воспроизводимым методом определения HbA1c является его определение с использованием оборудования фирмы «Био-Рад» (табл. 4).

Таким образом, для ранней диагностики нарушений углеводного обмена (эпидемиологические исследования, беременность и др.) и диабета, мониторинга состояния компенсации заболевания, наряду с определением гликемии натощак, необходимо определение содержания гликозилированного гемоглобина в крови.
Контроль гликемии является дорогостоящим, и расходы на его осуществление значительно выше, чем приобретение сахароснижающих препаратов. Несмотря на это, проведение постоянного мониторирования за состоянием углеводного обмена у больных СД диктует тот факт, что профилактика сосудистых осложнений, отсрочка их развития и прогрессирования сохраняют работоспособность больных, их качество жизни и снижение частоты инвалидизации, расходы на которые значительно превышают те, которые направлены на постоянный контроль гликемии. Последние рекомендации ВОЗ, Международной федерации диабета, Европейской ассоциации по изучению СД, а также ООН еще раз подчеркивают необходимость своевременной диагностики данного заболевания, что возможно лишь при использовании современной диагностической аппаратуры, при лечении и проведении постоянного качественного контроля за терапией и профилактикой сосудистых осложнений СД.
По вопросам литературы обращайтесь в редакцию.
М. И. Балаболкин, доктор медицинских наук, профессор, академик РАЕН
Е. М. Клебанова, кандидат медицинских наук
А. В. Ильин, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
