Лечащий Врач #4, 2008
Роль цефалоспоринов в антибактериальной терапии обострений хронической обструктивной болезни легких в амбулаторной практике
Хроническая обструктивная болезнь легких (ХОБЛ) представляет одну из ведущих причин смертности и растущих экономических потерь системы здравоохранения во всем мире. Развитие обострений заболевания часто служит основной причиной обращений за медицинской помощью, госпитализаций и летальных исходов. Согласно статистическим данным в США с ХОБЛ ежегодно связано более 165 000 смертей, 10 миллионов случаев обращений за медицинской помощью, более 2 миллионов госпитализаций, основной причиной которых является развитие обострений заболевания [1, 2, 3]. Большинство обострений ХОБЛ (около 80%) имеют инфекционную природу. При этом грамположительные и грамотрицательные бактерии вызывают 40–60% обострений, на долю вирусов и атипичной микрофлоры приходится около 30% и 5–10% соответственно [4, 5].
Наиболее часто определяемыми возбудителями при обострениях ХОБЛ легкой и средней тяжести являются Haemophilus influenzae, Streptococcus pneumoniae и Moraxella catarrhalis [6]. Убедительные доказательства относительно важности роли бактериальных инфекций в отношении причины обострений ХОБЛ были получены в исследовании Sethi и соавт. [7]. Авторами было показано, что обострения ХОБЛ в два раза чаще развиваются при инфицировании больных новыми штаммами H. influenzae, St. pneumoniae или M. catarrhalis. Так, 33% от общего количества обострений было связано с новыми штаммами и только в 15,4% обострений не было выявлено новых штаммов. Причинами тяжелых, требующих госпитализации обострений ХОБЛ, как правило, являются грамотрицательные микроорганизмы, такие как Klebsiella pneumoniae, Pseudomonas aeruginosa [8]. Механизм развития обострений ХОБЛ при инфицировании новыми штаммами детально не изучен. Наиболее вероятно, что иммунной системе организма не удается распознать новые штаммы уже известных возбудителей, что позволяет бактериям колонизировать слизистую, приводя к развитию клинических симптомов обострения. Возможно, новые штаммы обладают большей инвазивной активностью, вызывая повреждения слизистой, и развитие выраженной воспалительной реакции [9].
Данные о резистентности трех основных патогенов изменяются в зависимости от географического положения страны и времени проведения эпидемиологических исследований. Результаты исследования Alexander Project, проводимого в 26 странах мира на протяжении трех лет (1998–2000), свидетельствуют о том, что в среднем 19,6% штаммов H. influenzae продуцируют β-лактамазы, при этом в России данный показатель составил 4,2%, в США — 29,6%) [10] (табл. 1). Чувствительными к пенициллину оказались 93,8% российских штаммов St. pneumoniae.
Наиболее активными антибактериальными агентами по отношению к H. influenzae, по результатам исследования Alexander Proeject (уровень чувствительности более 97,5%), являются амоксициллин/клавуланат, цефиксим, азитромицин и респираторные фторхинолоны.
Сходные результаты относительно резистентности H. influenzae были получены по итогам программы SENTRY (1999–2003 гг.) [11]. Все выделенные штаммы M. catarrhalis оказались чувствительны к амоксициллину/клавуланату, цефиксиму и респираторным фторхинолонам. Наиболее существенные различия относительно географических регионов были зафиксированы в отношении S. pneumoniae. По результатам Alexander Proeject, в целом по миру уровень резистентности St. pneumoniae к пенициллину составил 10% (наиболее высокий уровень в Гонконге — 69,9%, наименьший в Нидерландах и Бразилии — 1,1%); резистентность к макролидам (эритромицину) составила 24,6%. Однако в ряде исследований, опубликованных в последние годы, приводятся данные о снижении количества пенициллин-резистентных штаммов пневмококка до 4,7–7% [12]. Несмотря на то, что снижение уровня пенициллин-резистентности ассоциируется с параллельным ростом чувствительности к цефалоспоринам и макролидам, уровень чувствительности к респираторным фторхинолонам начинает снижаться, что связывают с увеличением частоты их использования в популяции.
Современные рекомендации по лечению ХОБЛ (GOLD, 2006 [13]) свидетельствуют о необходимости применения антибиотиков при обострении ХОБЛ в следующих клинических ситуациях:
-
При наличии трех кардинальных признаков обострения: усилении одышки, увеличении объема выделяемой мокроты, гнойном характере мокроты (уровень доказательности В).
-
При наличии двух кардинальных признаков обострения, причем обязательным является наличие гнойной мокроты (уровень доказательности С).
-
У пациентов с тяжелым обострением ХОБЛ, требующим проведения механической вентиляции легких (инвазивной или неинвазивной (уровень доказательности В).
Наличие у пациента таких анамнестических факторов, как частые госпитализации, проведение более 4 курсов антибактериальной терапии за последний год, тяжелое обострение ХОБЛ, присутствие P. aeruginosa во время предыдущей госпитализации или в стабильном периоде, позволяет говорить о высоком риске выявления P. aeruginosae как причины настоящего обострения [14]. В табл. 2 представлена стратификация пациентов по возможным возбудителям обострений ХОБЛ в зависимости от тяжести обострения и наличия неблагоприятных прогностических факторов.
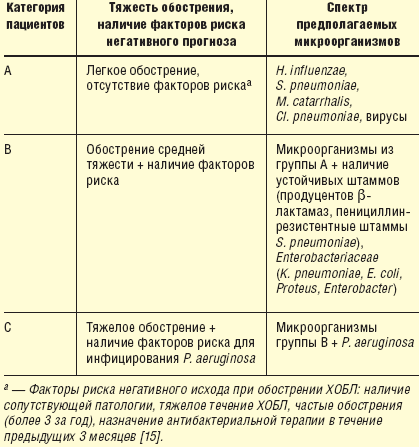
В табл. 3 представлены все классы антибактериальных препаратов, рекомендованных на сегодняшний день для лечения обострений ХОБЛ в зависимости от тяжести обострения, а также пути введения препарата. При этом пероральный путь введения всегда предпочтительнее. Основываясь на результатах проведенных клинических исследований, курс антибактериальной терапии при обострениях ХОБЛ должен составлять от 3 до 7 дней (уровень доказательности D). При этом основными параметрами эффективности антибактериальной терапии являются стабилизация состояния больного, улучшение функции легких (возврат к базовым значениям), микробиологическая эрадикация возбудителя.

Принимая во внимание рекомендации по лечению ХОБЛ [13] и данные исследований по резистентности респираторных патогенов, цефалоспорины III поколения для перорального приема могут быть отнесены к препаратам первого выбора при обострениях ХОБЛ легкой и средней степени тяжести без признаков инфицирования P. aeruginosa. Данный класс антибактериальных препаратов, наряду с оптимальными фармакокинетическими параметрами и режимом дозирования, обладает высокой стабильностью в отношении β-лактамаз H. influenzae, M. catarrhalis, улучшенной активностью в отношении пенициллин-чувствительных штаммов пневмококка и метициллин-чувствительных S. aureus. Перечисленные факторы определяют несомненные терапевтические преимущества по отношению к традиционным антибиотикам для перорального приема (амоксициллин, триметоприм/сульфаметаксазол, тетрациклин, эритромицин) [16].
Модификация химического ядра цефалоспоринов I поколения привела к появлению новых полусинтетических цефалоспоринов для перорального и парентерального приема. Ранние генерации пероральных цефалоспоринов (цефалексин, цефрадин) обладали ограниченной активностью против грамотрицательных микроорганизмов и невысокой стабильностью в отношении b-лактамаз. Целенаправленные модификации химической структуры привели к появлению генерации пероральных широкого спектра антибактериальной активности цефалоспоринов III поколения (цефдинир, цефтибутен, цефиксим, цефподоксим) [17]. Цефалоспорины третьего поколения имеют аминотиазолиловый цикл в боковой цепи 7-й позиции, гарантирующий более высокую стабильность к β-лактамазам, по сравнению с цефалоспоринами I и II поколений. Эти молекулы более активны против грам отрицательных микроорганизмов, в особенности против Enterobacteriaceae. Одним из представителей пероральных цефалоспоринов III поколения является цефиксим. Цефиксим обладает улучшенной стабильностью к действию β-лактамаз и высокой активностью против основных респираторных патогенов [18]. Кроме аминотиазолилового цикла, в 7-й позиции боковой цепи этот препарат имеет метоксиимино-группу, которая повышает устойчивость к b-лактамазам, синтетизируемым грамотрицательными бактериями. Винильная группа в третьей позиции обеспечивает как хорошее всасывание этого антибиотика, так и другие фармакокинетические параметры. С другой стороны, по сравнению с предыдущими производными, эта группа ослабляет активность этого цефалоспорина к стафилококкам.
С целью оптимального выбора антибиотика для лечения обострения ХОБЛ необходимо учитывать:
-
активность препарата in vitro (естественная и индуцированная резистентность);
-
фармакокинетику;
-
спектр побочных эффектов;
-
бактерицидный эффект в месте инфекции (фармакодинамический эффект in vivo).
При применении β-лактамов (пенициллинов, цефалоспоринов и карбапенемов) клиническое и бактериологическое излечение определяется тем, что концентрации антибиотика в сыворотке и в месте инфекции должны на 40–50% превосходить значение МПК для данного патогена (С > МПК).
Исследования, проведенные на здоровых добровольцах, показывают, что биодоступность цефиксима составляет примерно 50%. Цефиксим обладает оптимальными фармакокинетическими параметрами: после приема внутрь дозы в 400 мг максимальная концентрация в сыворотке (2,6–4,8 мг/л, средняя концентрация — 3,7 мг/л) достигается спустя 3–4 часа. При приеме препарата с пищей несколько удлиняется время достижения максимальной концентрации. Концентрация цефиксима в слизистой бронхов составляет 51–82% его концентрации в сыворотке, а в выделениях бронхов и в мокроте — несколько ниже (10–20% и 4%). После приема внутрь дозы в 400 мг концентрация цефиксима в слизистой бронхов значительно превышает значения МПК ряда бактерий, играющих роль в развитии обострений ХОБЛ [19]. Фармакокинетические исследования показывают, что за 15-дневный период приема цефиксима (400 мг/л) не отмечалось ни накопления, ни понижения уровня цефиксима в сыворотке. Выведение препарата с мочой было равномерным. Лишь при тяжелой почечной недостаточности (клиренс креатинина ниже 20 мл/мин) следует понизить дозу. Нет необходимости изменять дневную дозу препарата у пожилых больных [20]. Кроме того, было установлено, что для трех патогенов, наиболее часто вызывающих внебольничные инфекции нижних дыхательных путей (H. influenzae, S. pneumoniae и M. catarrhalis), С > МПК превосходит 50%. Также важно отметить, что после приема внутрь дневной дозы в 400 мг концентрация препарата в сыворотке в течение 24 часов значительно превышает значения МПК90 для H. influenzae (табл. 4).
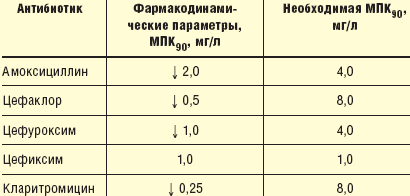
Данные многочисленных исследований подтверждают, что относительно длительное время полувыведения цефиксима, а также его фармакокинетический/фармакодинамический профиль по отношению к ряду патогенов (H. influenzae, E. coli, K. peumoniae, M. catarrhalis, N. gonorrhoeae, P. mirabilis, St. pneumoniae, St. spyogenes) позволяют клиницистам широко использовать этот антибиотик.
Эффективность цефиксима в терапии обострений ХОБЛ подтверждена в нескольких клинических исследованиях [21, 22, 23]. В большинстве клинических исследований был использован цефиксим в дозе 400 мг однократно в течение 10–14 дней. Исследование Stratton и соавт., включавшее 1322 пациента с обострением ХОБЛ, доказало клиническую эффективность 7-дневного курса лечения [24]. Lorenz и соавт. провели двойное слепое, плацебо-контролируемое, рандомизированное исследование по оценке эффективности 5-дневного курса цефиксима в сравнении с традиционным 10-дневным при обострениях ХОБЛ [25] (табл. 5).
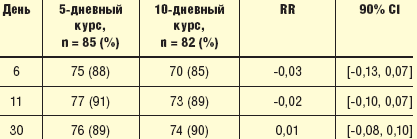
Анализ результатов исследования показал, что клиническая эффективность на 11 сутки была сопоставимой в обеих группах, кроме того, уже на 6 день исследования клиническая эффективность в группе 5-дневной терапии составила 88%, 85% в группе сравнения. К 30-му дню исследования клиническая эффективность была сходной в обеих группах (89 и 90% соответственно). Микробиологическая эффективность также оказалась одинаковой в обеих группах, достигнув к 11 суткам 71% в группе 5-дневной терапии и 82% в группе 10-дневной терапии (p > 0,05) (табл. 6). В обеих группах к 11 дню наблюдения произошло достоверно снижение уровня С-реактивного белка, что свидетельствует о снижении интенсивности воспалительного процесса.

Результаты данного исследования свидетельствуют, что клиническая и микробиологическая эффективность 5-дневного курса цефиксима сопоставима с 10-дневным курсом. Цефиксим хорошо переносился пациентами обеих групп, нарушения со стороны желудочно-кишечного тракта (13 и 18% пациентов из каждой группы) были отмечены как возможно связанные с приемом препарата. Сокращение продолжительности курса антибактериальной терапии повышает приверженность больного лечению и является более выгодным с фармакоэкономической точки зрения.
Постоянные колебания уровня резистентности респираторных патогенов определяют необходимость проведения локальных эпидемиологических исследований и предъявляют высокие требования к эффективности антибактериальных препаратов, используемых для эмпирической терапии обострений ХОБЛ. В настоящее время наиболее часто рекомендуется применение b-лактамных антибиотиков и макролидов, предпочтение отдается препаратам для перорального приема. Пероральные цефалоспорины III поколения, характеризующиеся оптимальным фармакокинетическим/фармакодинамическим профилем, широким спектром антибактериальной активности, коротким курсом и удобством приема, обладают прекрасными возможностями для амбулаторной терапии обострений ХОБЛ средней тяжести.
По вопросам литературы обращайтесь в редакцию.
А. Н. Цой, доктор медицинских наук, профессор
Н. Б. Лазарева, кандидат медицинских наук
В. В. Архипов, кандидат медицинских наук
Ю. А. Антоновский
ММА им. И. М. Сеченова, ГКБ № 23 им. «МЕДСАНТРУД», Москва
