Лечащий Врач #6, 2008
Динамика пульсового давления на фоне лечения амлодипином и карведилолом у больных артериальной гипертонией
Пульсовое давление (ПД), отражая эластические свойства магистральных сосудов и функцию левого желудочка сердца [9], представляет собой важнейший параметр гемодинамики, простой и доступный при измерении на плечевой артерии. Исследования последнего десятилетия убедительно продемонстрировали неблагоприятное прогностическое значение периферического ПД в увеличении риска сердечно-сосудистой заболеваемости и смертности [3, 11, 13]. Это позволило экспертам Европейского общества по артериальной гипертонии (АГ) (ESH) в 2007 г. впервые отнести высокое ПД к факторам риска неблагоприятного прогноза у больных АГ старшего возраста [5].
Между тем в ряде клинических исследований было продемонстрировано отсутствие строгого параллелизма в степени снижения систолического (САД) и диастолического артериального давления (ДАД) на фоне гипотензивной терапии. Это может привести, в первую очередь, к нормализации ДАД, в то время как САД и ПД останутся неизмененными [7]. По некоторым данным, «сверхнормализация» ДАД вызывает прирост ПД, что может увеличивать сердечно-сосудистый риск [15]. Вместе с тем динамика ПД на фоне гипотензивной терапии до сих пор остается малоизученной. Соответственно, не разработаны и клинические рекомендации по «прицельному» снижению ПД.
Это определило цель работы: на фоне гипотензивной медикаментозной терапии амлодипином и карведилолом изучить динамику пульсового артериального давления (АД) во взаимной связи с жесткостью магистральных сосудов эластического типа у больных АГ пожилого и старческого возраста.
Материал и методы. Динамику ПД на фоне гипотензивного лечения изучали в двух подгруппах. В первой исследовали влияние блокатора медленных кальциевых каналов амлодипина, во второй — комбинированного альфа- и бета-адреноблокатора карведилола.
До начала исследования в случаях постоянного приема гипотензивных средств пациентам отменяли лечение на срок от 3 до 7 дней, но не менее чем на пять периодов полувыведения. По окончании «отмывочного» периода проводили суточное мониторирование АД (СМАД). Критериями включения были возраст старше 60 лет, уровень среднесуточного САД ≥125 мм рт. ст. и отсутствие противопоказаний к бета-адреноблокаторам или антагонистам кальция.
В подгруппу амлодипина было отобрано 30, в подгруппу карведилола — 50 пациентов. Подгруппы рандомизировали по методу конвертов, после чего открытым способом назначали амлодипин (Нормодипин®, «Гедеон Рихтер», Венгрия) в стартовой дозе 5 мг/сут или карведилол (Акридилол®, «Акрихин», Россия) в стартовой дозе 25 мг/сут. Каждые две недели проводили повторные осмотры, включающие контроль АД, частоты сердечных сокращений (ЧСС), регистрацию побочных эффектов и нежелательных явлений. В случаях недостижения целевого уровня офисного АД (< 140/90 мм рт. ст.) через две недели от начала лечения, дозы препаратов увеличивали вдвое (карведилол — до 50 мг/сут, амлодипин — до 10 мг/сут). Через 4 недели больным, не достигшим целевого уровня АД, к терапии добавляли ретардную форму индапамида в дозе 1,5 мг/сут, после чего лечение продолжали до восьми недель. По окончании восьминедельного курса всем пациентам осуществляли повторное СМАД.
Восьминедельный курс лечения закончили 69 человек: 26 — в подгруппе амлодипина и 43 — карведилола. Подгруппы были сопоставимы по полу, возрасту, исходным среднесуточным уровням САД, ДАД, ПД. ЧСС преобладала в подгруппе карведилола (табл. 1).
Исходно и по окончании курса лечения в каждой подгруппе рассчитывали и сравнивали следующие показатели:
-
cреднесуточные уровни САД, ДАД и ЧСС; cреднесуточные, среднедневные и средненочные значения ПД;
-
индекс AASI (Ambulatory Arterial Stiffness Index) как суррогатный маркер жесткости аорты и крупных сосудов эластического типа, который определяли по следующей методике. Для каждого пациента с помощью линейного регрессионного анализа устанавливали степень взаимосвязи САД и ДАД, полученных при СМАД. AASI считали по формуле: AASI = 1 — B, где B — коэффициент линейной регрессии [6];
-
кратковременные экстремальные подъемы АД (КЭПАД). С этой целью анализировали полученные при СМАД суточные кривые АД. Критерием кратковременных подъемов считали одновременное наличие двух признаков: 1) максимум САД и/или ДАД выше индивидуального среднедневного или средненочного значения АД на 2 и более стандартных отклонения; 2) максимум САД ≥ 140 и/или максимум ДАД ≥ 90 мм рт. ст. Началом КЭПАД считали момент перехода ЧСС, САД и ДАД от стабильного состояния на графике СМАД к их динамике в виде тренда [2]. Учитывали пиковые уровни ПД, САД, ДАД и ЧСС. Проводили сравнительный анализ динамики указанных параметров.
Так как распределение признаков отличалось от нормального, применяли непараметрические методы статистики. Средние значения отображали в виде медиан (Ме) с интерквартильным интервалом (ИИ). Статистическую значимость различий в независимых выборках определяли по Манну–Уитни, в зависимых — по Вилкоксону. Для сравнения групп по качественному признаку использовали критерий χ2.
Результаты
Средняя курсовая доза амлодипина составила 9,2 ± 1,8 мг/сут. При этом 5 мг амлодипина в течение всего курса лечения принимали 4 пациента (15,4%), у 22 (84,6%) суточная доза была увеличена до 10 мг. Комбинация амлодипин + индапамид использовалась у 4 больных (15,4%). Доза карведилола к окончанию 8-недельного периода составляла 40,1 ± 13,2 мг. У 14 пациентов (32,6%) — 25 мг/сут, у 27 (62,8%) — увеличена до 50 мг/сут. В двух случаях, в связи с брадикардией, суточная доза была уменьшена до 12,5 мг, при этом был добавлен индапамид. Всего комбинация карведилол + индапамид была назначена 20 пациентам (46,5%).
В табл. 2 приведены параметры СМАД и индексы AASI исходно и после 8 недель приема препаратов.
Как видно, на фоне приема амлодипина и карведилола показатели САД, ДАД и ПД достоверно снизились. В то же время не выявлено динамики ЧСС при использовании амлодипина, в отличие от карведилола, где отмечалось значимое урежение пульса.
Степень уменьшения среднесуточного ПД в подгруппе амлодипина составила 5,1 мм рт. ст. (8,3%), падение ПД зафиксировано в 22 случаях из 26 (84,6%), отсутствие динамики или его рост — у 4 больных (15,4%). В подгруппе карведилола ПД в среднем уменьшилось на 3,0 мм рт. ст. (6,0%), снижение ПД отмечено у 30 пациентов (69,8%), отсутствие динамики или его рост — у 13 (30,2%). Изменений жесткости аорты по индексу AASI в обеих подгруппах не отмечалось.
Перед началом приема амлодипина у 25 из 26 больных было выделено 68 КЭПАД (в среднем, по 2,7 за сутки мониторирования). После 8 недель лечения обнаружено 54 эпизода АГ у 25 пациентов. Среднее количество кратковременных подъемов АД за сутки уменьшилось до 2,2. В подгруппе карведилола исходно по суточным записям АД было выделено 90 КЭПАД у 42 пациентов (по 2,1 за сутки мониторирования). По истечении 8 недель приема карведилола обнаружено 75 эпизодов АГ у 38 пациентов (2,0 за сутки).
В табл. 3 приведены пиковые значения САД, ДАД, ПД и ЧСС на фоне приема препаратов.
Как оказалось, применение амлодипина приводило к достоверному снижению пиковых САД, ДАД и ПД. Максимальная ЧСС при этом не изменялась. Прием карведилола сопровождался снижением пиковых ДАД и ЧСС. Однако максимальные значения САД и ПД не изменились.
Сравнительная характеристика динамики показателей СМАД по результатам лечения амлодипином и карведилолом отображена в табл. 4.
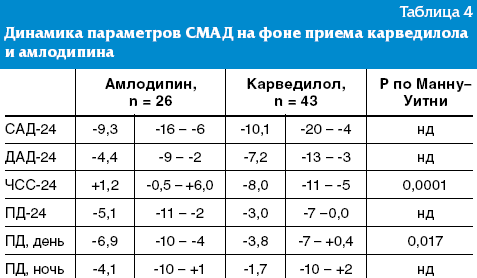
Из таблицы следует, что амлодипин, по сравнению с карведилолом, в большей степени снижал уровень дневного ПД. Величина снижения среднесуточной ЧСС преобладала в подгруппе карведилола.
Обсуждение
Выбор препаратов для исследования был обусловлен наличием у амлодипина и карведилола отчетливого вазодилатирующего эффекта, что вызывает снижение диастолического АД. При этом механизмы влияния на тонус периферических сосудов у препаратов принципиально различаются: амлодипин оказывает прямое расслабляющее воздействие на гладкую мускулатуру сосудов [1], а карведилол обладает альфа-адреноблокирующей активностью [4]. Падение ДАД может закономерно приводить к увеличению ПД. Сравнительный анализ динамики ПД на фоне приема амлодипина и карведилола у больных АГ во взаимосвязи с жесткостью аорты ранее не проводился.
Результаты показали, что амлодипин и карведилол при курсовом приеме в одинаковой степени снижали среднесуточное САД и ДАД. Различной, как и ожидалось, была динамика ЧСС: при использовании карведилола отмечалось ее достоверное урежение, на фоне амлодипина — отсутствие сдвигов в частоте пульса. Наши данные согласуются с результатами субисследования CAFE-ASCOT, где гипотензивная терапия на основе атенолола приводила к уменьшению ЧСС в среднем на 13,2 мин-1, в то время как комбинация на основе амлодипина — всего на 2,6 мин-1 [16].
Сравнительный анализ продемонстрировал в два раза большую активность амлодипина по снижению дневного ПД, по сравнению с карведилолом (на 6,9 и 3,8 мм рт. ст. соответственно). Более того, в 30,2% случаев на фоне приема последнего отмечен рост ПД или отсутствие его динамики (в подгруппе амлодипина таких больных было вдвое меньше — 15,4%). Наши данные подтвердили сведения зарубежных исследователей о депрессорном влиянии амлодипина на уровень ПД [10, 12]. Изменения ПД при приеме карведилола исследованы в единичных работах. Их итоги оказались разноречивыми. По одним данным препарат достоверно снижал среднесуточное ПД [8], что согласуется с нашими результатами. По сведениям других авторов, прием карведилола у больных сердечной недостаточностью приводил к увеличению ПД [14].
Каковы вероятные причины меньшего влияния карведилола на уровень периферического ПД, по сравнению с амлодипином? Во-первых, возможно неодинаковое воздействие препаратов на жесткость аорты и крупных сосудов эластического типа. По нашим данным индекс AASI не изменялся в обеих подгруппах, что указывает на отсутствие динамики жесткости аорты. Аналогичные результаты при лечении амлодипином и атенололом получены в исследовании CAFE-ASCOT, где сосудистая жесткость оценивалась по скорости распространения пульсовой волны [16]. Во-вторых, причиной недостаточного снижения ПД может быть периферический вазоспазм, увеличивающий отраженную пульсовую волну. Однако карведилол, в отличие от большинства других бета-адреноблокаторов, обладает вазодилатирующим эффектом, что косвенно подтверждается выраженным (на 7,2 мм рт. ст.) снижением ДАД в подгруппе карведилола. По литературным сведениям карведилол в большей степени уменьшал ДАД, чем метопролол [14].
Таким образом, можно согласиться с мнением группы исследователей CAFE-ASCOT Trial о том, что наиболее вероятной причиной различного влияния режимов терапии, основанных на антагонисте кальция и бета-адреноблокаторе, является значимое замедление ЧСС под воздействием последнего [16]. Урежение пульса, с одной стороны, приводит к увеличению ударного объема, с другой — обусловливает возвращение отраженной пульсовой волны в систолу. Это может ослаблять эффективность снижения ПД в аорте под влиянием бета-адреноблокаторов.
Нами впервые изучены параметры кратковременных подъемов АД на фоне гипотензивного медикаментозного лечения. Под влиянием карведилола пиковые ПД и САД не изменялись, несмотря на уменьшение среднесуточных показателей СМАД. В то же время значительно снизилась максимальная ЧСС. Можно предполагать, что в условиях экстремальных повышений АД влияние карведилола на ПД и САД выражено в меньшей степени, что обусловлено урежением пульса на максимуме АД. Напротив, прием амлодипина приводил к достоверному снижению ПД и САД на высоте кратковременных эпизодов АГ. Это может уменьшать динамическую прессорную нагрузку на органы-мишени.
Выводы
Таким образом, при восьминедельном курсе лечения антагонист кальция амлодипин, в отличие от комбинированного адреноблокатора карведилола, приводит к большему снижению среднедневного ПД, уменьшению пульсового и систолического АД на высоте кратковременных эпизодов АГ и не влияет на уровень ЧСС. Амлодипин может быть рекомендован как один из гипотензивных препаратов для целенаправленного снижения ПД у больных АГ пожилого и старческого возраста.
Литература
-
Галявич А. С. Антагонисты кальция при лечении артериальной гипертонии // Руководство по артериальной гипертонии /
Под ред. Чазова Е. И. М.: Медиа Медика, 2005. С. 634–643. -
Куклин С. Г. Краткосрочная нестабильность при гипертонической болезни (Анализ. Прогноз). Иркутск: Изд-во Иркутского ГИУВа. 2003. 200 c.
-
Оганов Р. Г. Профилактическая кардиология: от гипотез к практике // Кардиология. 1999. Т. 39. № 2. С. 4–9.
-
Рациональная фармакотерапия сердечно-сосудистых заболеваний: Рук. для врачей. Под ред. Чазова Е. И., Беленкова Ю. Н. М.: Литтерра, 2004. 972 с.
-
2007 Guidelines for the management of arterial hypertension. The task force for the management of arterial hypertension of the ESH and ESC // J. Hypertens. 2007. Vol. 25, № 6. P. 1105–1187.
-
Li Y., Wang J. G., Dolan E. et al. Ambulatory arterial stiffness index derived from 24-hour ambulatory blood pressure monitoring // Hypertension. 2006. Vol. 47, № 3. P. 359–364.
-
Black H. R. The paradigm has shifted to systolic blood pressure // Hypertension. 1999. Vol. 34. P. 386–387.
-
Weber M. A., Sica D. A., Tarka E. A. et al. Controlled-release carvedilol in the treatment of essential hypertension // Am. J. Cardiol. 2006. Vol. 98. P. 32L–38L.
-
Dart A. M. Pulse pressure–a review of mechanisms and clinical relevance // J. Am. Coll. Cardiol. 2001. Vol. 37. P. 975–984.
-
Ruilope L. M., Malacco E., Khder Y. et al. Efficacy and tolerability of combination therapy with valsartan plus hydrochlorothiazide compared with amlodipine monotherapy in hypertensive patients with other cardiovascular risk factors: the VAST study // Clin. Ther. 2005. Vol. 27. P. 578–587.
-
Franklin S. S. Hypertension in Older People: Part 1 // J. Clin. Hypertens. 2006. Vol. 8, № 6. P. 444–449.
-
London G., Schmieder R., Calvo C., Asmar R. Indapamide SR versus candesartan and amlodipine in hypertension: the X-CELLENT Study // Am. J. Hypertens. 2006. Vol. 19. P. 8–9.
-
Franklin S. S., Khan S. A., Wong N. D. et al.Is pulse pressure useful in predicting risk of coronary heart-disease? The Framingham Heart Study // Circulation. 1999. Vol. 100. P. 354–360.
-
Azevedo E. R., Kubo T., Mak S. et al. Nonselective versus selective ?-adrenergic receptor blockade in congestive heart failure: differential effects on sympathetic activity // Circulation. 2001. Vol. 104. P. 2194–2199.
-
Safar M. E., Blacher J., Mourad J. J. et al. What does STOP-2 tell us about management of hypertension? // Lancet. 2000. Vol. 355. P. 651–653.
-
Williams B. Differential impact of blood pressure-lowering drugs on central aortic pressure and clinical outcomes: principal results of the Conduit Artery Function Evaluation (CAFE) study // Circulation. 2006. Vol. 113. P. 1213–1225.
А. А. Дзизинский, доктор медицинских наук, профессор, член-корреспондент РАМН
К. В. Протасов, кандидат медицинских наук, доцент
О. В. Федоришина
ИГИУВ, Иркутск
