Лечащий Врач #10, 2008
Проблемы применения диуретиков у пациентов с артериальной гипертонией и метаболическими нарушениями
Диуретики для лечения артериальной гипертензии (АГ) используются с конца 50-х годов прошлого века. Известно, что они способны улучшать отдаленный прогноз у больных АГ. Кроме того, тиазидные диуретики усиливают эффективность других антигипертензивных препаратов и поэтому хорошо подходят для комбинированной терапии АГ [3–7].
Антигипертензивная терапия, назначаемая врачами, далеко не всегда бывает оптимальной. Очень часто назначаются лекарственные средства, не рекомендованные для длительного лечения АГ. Во всем мире стало типичным преимущественное назначение относительно новых антигипертензивных препаратов (присутствующих на фармацевтическом рынке не более 10–15 лет). Вероятно, это происходит потому, что под воздействием фармацевтических компаний дорогостоящие лекарственные средства вытесняют более старые и недорогие [13–16]. Однако подобная тенденция не обоснована данными доказательной медицины. Сравнительные исследования (HANE, 1997; САРРР, 1999; SТОР-2, 1999; ALLHAT, 2002; NORDIL, 2000) не показали преимуществ блокаторов кальциевых каналов и ингибиторов АПФ по сравнению с тиазидовыми и тиазидоподобными диуретиками в снижении артериального давления (АД), в профилактике осложнений и в уменьшении смертности у больных с АГ. Рандомизированное, многоцентровое, двойное слепое клиническое исследование ALLHAT, проведенное в США, было важной вехой изучения сравнительной эффективности разных групп антигипертензивных средств. В исследовании сравнивалась эффективность и безопасность ингибиторов АПФ, блокаторов кальциевых каналов, тиазидовых диуретиков и альфа-адреноблокаторов у пациентов с АГ и высоким риском осложнений [3]. Исследование было длительным (4–8 лет наблюдения) и включало большое количество пациентов (в каждой группе было от 9000 до 15000 участников). Полученные результаты были достаточно неожиданными. Было выявлено, что тиазидовые диуретики не уступает по эффективности ингибиторам АПФ и блокаторам кальциевых каналов, а по некоторым показателям даже превосходит их. Полученные результаты актуализировали использование тиазидовых диуретиков в лечении АГ. Данные, полученные в исследовании ALLHAT, подтверждают результаты ранее проведенного систематического обзора, показавшего, что использование тиазидовых и тиазидоподобных диуретиков в качестве препаратов первого выбора при АГ в сравнении с плацебо или отсутствием терапии достоверно эффективно, снижает АД и уменьшает риск развития серьезных осложнений и смерти [2].
Тиазидовые и тиазидоподобные диуретики широко используются как антигипертензивные средства во всем мире уже более 50 лет. Препараты этой группы внедрялись в клиническую практику в определенном хронологическом порядке: в 1956 г. — хлортиазид, в 1957 г. — гидрохлортиазид, в 1959 г. — хлорталидон, в 1974 г. — индапамид.
Важнейшее преимущество тиазидовых диуретиков перед другими классами антигипертензивных препаратов— их низкая стоимость, которая делает возможным широкое использование диуретиков в качестве начальной терапии АГ у больных с низкими доходами. Однако пациенту нельзя назначать препарат, основываясь только на цене и общих эффектах, свойственных тиазидовым и тиазидоподобным диуретикам. Если оценивать эффективность и безопасность внутри этой фармакологической группы, препаратом выбора, несомненно, является индапамид, который превосходит другие диуретики по антигипертензивной эффективности, лучше переносится и не вызывает существенных нарушений пуринового, углеводного и липидного обмена [1, 8–11].
Согласно данным, приведенным в Государственном реестре лекарственных средств РФ, индапамид— гипотензивное средство, по фармакологическим свойствам близкое к тиазидным диуретикам. Препарат увеличивает выведение с мочой Na+, Cl- и в меньшей степени K+ и Mg2+. Обладая способностью селективно блокировать «медленные» кальциевые каналы, индапамид повышает эластичность стенок артерий и снижает общее периферическое сопротивление. Кроме того, препарат способствует уменьшению гипертрофии левого желудочка сердца, не влияет на содержание липидов в плазме; не влияет на углеводный обмен (в том числе у больных с сопутствующим сахарным диабетом), снижает чувствительность сосудистой стенки к норадреналину и ангиотензину II, стимулирует синтез PgE2 и простациклина PgI2, снижает продукцию свободных и стабильных кислородных радикалов. При назначении в высоких дозах индапамид не влияет на степень снижения АД, несмотря на увеличение диуреза. Антигипертензивный эффект препарата развивается постепенно, что заметно уменьшает риск гипотензивных реакций. После многократного приема терапевтический эффект индапамида отмечается через 1–2 недели, достигает максимума к 8–12 неделе и сохраняется до 8 недель.
Индапамид рекомендуется для начальной терапии АГ современными международными и российскими экспертами, может быть использован в качестве препарата для комбинированной терапии АГ с любым другим классом антигипертензивных средств, обеспечивает эффективную органопротекцию больным с гипертрофией левого желудочка и микропротеинурией, имеет наилучшее соотношение эффективность/безопасность в сравнении с другими диуретиками, оказывает нейтральное влияние на липидный и углеводный обмен.
Однако на сегодняшний день для эффективного снижения АД большинству пациентов необходима комбинированная антигипертензивная терапия, поэтому, основываясь на сведениях о клинической фармакологии антигипертензивных препаратов и данных клинических исследований, возникает потребность выбрать оптимальную комбинацию для лечения артериальной гипертензии у пациентов, нуждающихся в комбинированном лечении.
Серьезной проблемой в настоящее время является метаболическая безопасность антигипертензивной терапии. Многие антигипертензивные препараты могут существенно влиять на липидный и углеводный обмен за счет различных механизмов (табл. 1).
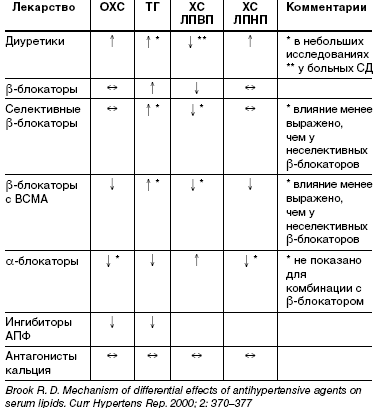
В журнале Lancet (2007) опубликован сетевой метаанализ клинических исследований эффективности и безопасности различных классов антигипертензивных средств, в котором оценивалось влияние препаратов на метаболизм [12]. Данные метаанализа свидетельствуют о наличии у средств, действующих на ренин-ангиотензиновую систему, положительного метаболического действия, что определяет их как наиболее перспективную группу для комбинирования с тиазидовыми и тиазидоподобными диуретиками. Однако клиническая целесообразность использования подобной комбинации у российских пациентов требует подтверждения в отечественных клинических исследованиях. Все вышесказанное послужило причиной проведения клинического исследования, целью которого было оценить метаболические эффекты двух вариантов комбинированной антигипертензивной терапии: совместного применения двух препаратов— ингибитора АПФ эналаприла в дозе 20 мг (Энапа), тиазидоподобного диуретика пролонгированного действия индапамида 1,5 мг (Равела СР) и фиксированной комбинации ингибитора АПФ эналаприла и тиазидового диуретика гидрохлоротиазида(Энапа-НЛ 20).
Материалы и методы
В исследование было включено 112 человек в возрасте от 18 до 65 лет, страдающих эссенциальной АГ. Критериями исключения были сахарный диабет, нарушение толерантности к углеводам, ишемическая болезнь сердца и ее эквиваленты.На первом, предварительном, этапе исследования выявлялись пациенты, нуждающиеся в назначении комбинированной терапии. В течение 2 недель пациенты получали Энап в дозе 5 мг в сутки, затем при отсутствии достижения целевого АД (140/90 мм рт. ст.) дозировка увеличивалась до 10 мг, а еще через 2 недели до 20 мг в сутки. У 36 пациентов нормализация АД была достигнута при монотерапии Энапом. 71 пациент, не достигший целевых цифр АД на монотерапии, был включен в основную часть исследования и переведен на комбинированную терапию. На этом этапе пациенты были методом «случай-контроль» разделены на две группы. Пациенты первой группы получали Энап 20 мг в комбинации с Равелом СР (35 чел.), пациенты второй группы— Энап-HЛ 20 (20 мг эналаприла малеата + 12,5 мг гидрохлоротиазида) (36 чел.). В качестве препарата, который добавлялся в случае не достижения целевых уровней АД, в обеих группах использовали метаболически нейтральный антигипертензивный препарат— амлодипин (Тенокс). Наблюдение продолжалось 6 месяцев с момента начала комбинированной терапии. Исследование завершили 66 человек. Приверженность к лечению была выше в группе, пациенты которой получали Энап-HЛ 20 (из 36 чел., включенных в исследование, выбыл 1 человек (2,7%)). Из группы (35 чел.), пациенты которой получали Энап в сочетании с Равелем СР, выбыло 4 человека (7%). Очевидно, это связано с меньшим количеством принимаемых таблеток в группе, где пациенты получали фиксированную комбинацию.
До начала комбинированной терапии, а также через 3 и через 6 месяцев контролировали гликемический профиль, креатинин крови, калий крови, инсулин крови, мочевую кислоту, общий холестерин (ОХС), триглицериды (ТГ), холестерин липопротеидов низкой плотности (ХС ЛПНП), холестерин липопротеидов высокой плотности (ХС ЛПВП), проводилось суточное мониторирование АД. Инсулинорезистентность оценивалась наиболее простым и удобным для применения в клинической практике методом— по изменению концентрации инсулина плазмы крови натощак. Известно, что гиперинсулинемия при нормогликемии, как правило, свидетельствует о наличии инсулинорезистентности. Трудность представляет стандартизация этого метода, поскольку нормальные значения инсулинемии крайне вариабельны. Предложены различные индексы для оценки инсулинорезистентности, рассчитываемые по соотношению концентраций инсулина и глюкозы плазмы натощак и/или после пищевой нагрузки. В нашем исследовании использовался один из таких общепринятых расчетных индексов— индекс HOMA-IR, разработанный D. Matthews: инсулин сыворотки натощак (мкед/мл) глюкоза плазмы натощак (ммоль/л)/22,5.
Индекс HOMA-IR был впервые описан в 1985 году и до сих пор широко используется во всем мире. Этот индекс коррелирует с более сложными методами определения инсулинорезистентности.
Характеристика пациентов, завершивших основной этап исследования, приведена в табл. 2. На этом этапе из исследования выбыли 5 человек, не соблюдавшие режим приема препарата. 66 пациентов завершили исследование.
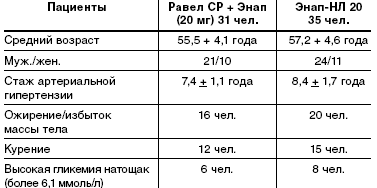
Анализируя результаты исследования, следует прежде всего отметить, что сформированные группы наблюдаемых были совершенно сопоставимы по данным комплексной оценки состояния сердечно-сосудистой системы и метаболических показателей во время первого визита.
В проведенном нами исследовании до начала комбинированной терапии в обеих группах было отмечено повышение средних значений систолического (САД) и диастолического АД (ДАД), индекса НОМА, ОХС, ХС ЛПНП по сравнению с нормой. Динамика показателей, изучавшихся в исследовании, приведена в табл. 3.
Динамика АД в двух группах достоверно не отличалась. Статистически значимое снижение АД наблюдалось уже через 3 месяца от начала комбинированной терапии. К концу 6 месяца терапии значение как САД, так и ДАД в обеих группах достигло нормальных цифр, что свидетельствует о высокой эффективности обеих комбинаций.
При оценке инсулинорезистентности в динамике было выявлено статистически значимое снижение индекса НОМА в группе, принимавшей Равел СР в комбинации с Энапом в дозе 20 мг, через 3 и 6 месяцев по сравнению с исходным уровнем (табл. 3). Во второй группе подобные изменения также наблюдались, но различия с исходным уровнем не достигли статистически значимого уровня.
Важным результатом нашего исследования было статистически значимое снижение уровня ОХ и ХС ЛПНП у пациентов, получавших Энап в комбинации с Равелем СР. Эти изменения наблюдались уже через 3 месяца от начала лечения и сохранялись через 6 месяцев, что свидетельствует о значимом положительном влиянии исследуемой комбинации на метаболический профиль. В группе, принимавшей Энап-HЛ 20, подобных изменений не наблюдалось, препарат проявил себя как метаболически нейтральный.
Чем же обусловлены полученные нами различия в метаболических эффектах двух комбинаций? Вероятно, это связано с тем, что в одном случае метаболически позитивное действие ингибитора АПФ нивелируется негативным влиянием тиазидового диуретика. Во втором случае метаболически нейтральный тиазидоподобный диуретик при сохранении антигипертензивной активности комбинации сохраняет метаболически позитивное действие ингибитора АПФ, что делает данную комбинацию наиболее приемлемой у больных с уже имеющимися метаболическими нарушениями.
Таким образом, комбинация Равела СР и Энапа в дозе 20 мг в течение 6 месяцев на фоне модификации образа жизни оказывает позитивное метаболическое действие, уменьшает инсулинорезистентность, улучшает липидный спектр, что обуславливает целесообразность применения этой комбинации у большой когорты пациентов с артериальной гипертензией— у больных с уже имеющимися метаболическими нарушениями или высоким риском их развития. Подводя итоги работы, отметим, что комбинация большой дозы ингибитора АПФ и низкой дозы тиазидного диуретика (Энап-HЛ 20) показала себя метаболически нейтральной.
Литература
-
Ames R. P. A comparison of blood lipid and blood pressure responses during the treatment of systemic hypertension with indapamide and with thiazides// American Journal of Cardiology. 1996;77 (6):12 B–16 B.
-
Wright J. M., Cheng-Han Lee, Chambers K. C. Systematic review of antihypertensive therapies: Does the evidence assist in choosing a first-line drug?// Canadian Medical Association Journal. 1999;161 (1):25–32.
-
Research Group. Major cardiovascular events in hypertensive patients randomized to doxazosin vs chlorthalidone: the Anti-hypertensive and Lipid-lowering Treatment to Prevent Heart Attack Trial (ALLHAT)// JAMA. 2000; 283: 1967–1975.
-
The ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. The Anti-hypertensive and Lipid-lowering Treatment to Prevent Heart Attack Trial: major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: the Anti-hypertensive and Lipid-lowering Treatment to Prevent Heart Attack Trial (ALLHAT)// JAMA. 2002; 288: 2981–2997.
-
Hansson L., Lindholm L. H., Niskanen L. et al. Effect of angiotensin-converting enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPP) randomized trial// Lancet. 1999; 353: 611–616.
-
Medical Research Council Working Party. MRC trial of treatment of mild hypertension: principal results// Br Med J (Clin Res Ed). 1985; 291:97–104.
-
SHEP Cooperative Research Group. Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension. Final results of the Systolic Hypertension in the Elderly Program (SHEP) // JAMA. 1991; 265: 3255–3264.
-
British national formulary, ‡‚ 51, march, 2006.
-
Elisaf M. S., Theodorou J., Pappas H., Papagalanis N., Katopodis K., Kalaitzidis R., Siamopoulos K. C. Effectiveness and metabolic effects of perindopril and diuretics combination in primary hypertension// Journal of human hypertension. 1999, Nov. Volume 13. Issue 11. P. 787–791.
-
Malini P. L., Strocchi E., Ricci C., Ambrosioni E. Indapamide or hydrochlorothiazide in hypertensive patients resistant to treatment with an angiotensin-converting enzyme inhibitor// CURR THER RES CLIN EXP. 1994. V.55. Issue 8, p. 932–937.
-
Elliott W. J., Weber R. R., Murphy M. B. A double-blind, randomized, placebo-controlled comparison of the metabolic effects of low-dose hydrochlorothiazide and indapamide. Journal of clinical pharmacology// Date of Publication. 1991. Aug. V. 31. Issue 8. P. 751–757.
-
Elliott W. J., Meyer P. M. Incident diabetes in clinical trials of antihypertensive drugs: a network meta-analysis// Lancet. Jan. 20, 2007; 369: 201–07.
-
Semenchenko M. Drugs and prescribing in Russia: the challenges of transition//International Journal of Risk and Safety in Medicine. 1998, v. 11.
-
Hogerzeil H. V. Teacher’s Guide to Good Prescribing/H. V. Hogerzeil, K. I. Barnes, R. H. Henning, Y. E. Kocabasoglu, H. Moller, A. J. Smith, R. S. Summers, T. P.G.M. de Vries// Geneva. World Health Organization— Department of Essential Drugs and Medicines Policy. 2001. 98 р.
-
Петрова Г. И. Мониторинг национальной лекарственной политики— результаты сравнения по странам региона— Болгария, Румыния, Македония, Босния-Герцеговина// Центральный европейский журнал по общественному здравоохранению. 2001. ‡‚ 9. С. 205–215.
-
Mandal S. C. Study of rational drug use profiles in an Non-Government Organization-Managed Health Center versus Private Health Practitioners// Improving use of medicines: Abstracts of second international conference. Thailand. 2004. P. 39.
О. Н. Ткачева, доктор медицинских наук, профессор А. Ю. Галяутдинова, кандидат медицинских наук МГМСУ, Москва
