Лечащий Врач #01, 2009
Часто болеющие дети: проблемы диагностики, патогенеза и терапии
Детей, подверженных частым острым респираторным заболеваниям (ОРЗ), принято называть часто болеющими (ЧБД). Иногда, для того чтобы подчеркнуть особенности течения респираторных инфекций у этих детей (их затяжной характер), используется термин «часто и длительно болеющие дети». В зарубежной литературе используется термин «пациенты с рекуррентными (т. е. повторными) ОРЗ». При этом, например, в Великобритании к группе детей с рекуррентными респираторными инфекциями относят пациентов, у которых ОРЗ повторяются в течение года более 8 раз.
Таким образом, ЧБД — это термин, обозначающий группу детей, характеризующуюся более высоким, чем их сверстники, уровнем заболеваемости острыми респираторными инфекциями. При этом к ЧБД относят детей, у которых частые ОРЗ возникают в силу эпидемиологических причин из-за транзиторных, корригируемых отклонений в защитных системах организма.
Надо отметить, что в детском возрасте среди всех заболеваний респираторного тракта отмечается абсолютное преобладание ОРЗ. На их долю приходится более 90% всех болезней респираторной системы у детей. Максимальная заболеваемость ОРЗ среди детей отмечается в возрасте от 6 месяцев до 6 лет и составляет от 4 до 6 заболеваний в год. Среди школьников заболеваемость снижается до 2–5 случаев в год, а среди подростков — не превышает 2–4 заболеваний на протяжении года. Это всеобщая закономерность, обусловленная особенностями локальных и общих механизмов защиты в раннем и дошкольном возрасте, и она прослеживается у детей во всех странах мира независимо от экономического уровня их развития. На рисунке приведены статистические данные МЗ РФ за 2002 год, отражающие типичную динамику уровня заболеваемости ОРЗ в детском возрасте.
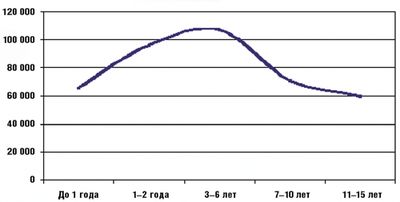
В отечественной педиатрии принято относить в группу ЧБД детей в зависимости от возраста и на основании критериев, предложенных А. А. Барановым и В. Ю. Альбицким (табл.).
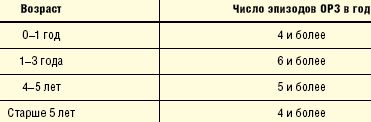
Распространенность ЧБД в детской популяции зависит, как уже упоминалось, от возраста, но также от эпидемиологических и социальных условий и составляет от 5 до 50% среди различных групп детей. Среди детей раннего возраста, посещающих детские сады, группа ЧБД может составлять около 40% и до 50%, в то время как среди школьников частые ОРЗ отмечаются менее чем у 15% детей и подростков. Отмечено, что среди ЧБД значительно чаще выявляются хронические заболевания носоглотки и легких, чаще встречается и тяжелее протекает бронхиальная астма, аллергический ринит, выше частота ревматизма, гломерулонефрита и ряда других заболеваний. Было также отмечено, что ЧБД в подростковом возрасте склонны к хроническим заболеваниям желудочно-кишечного тракта, сосудистым дистониям, у них легче развиваются невротические реакции, они быстрее утомляются, хуже учатся. Эта ситуация потенциально опасна с точки зрения формирования педагогических проблем (низкая успеваемость, отставание от учебной программы и т. д.). Кроме того, страдает психологический климат в семье. Так, установлено, что рекуррентные респираторные заболевания у детей более чем в 50% семей сопровождаются умеренным или значительным напряжением отношений между родителями и более чем в 57% — дефицитом внимания к другим членам семьи, в том числе и к другим детям. В целом показано, что более 70% родителей, дети которых часто болеют ОРЗ, констатируют ухудшение качества своей жизни.
Кроме того, частые ОРЗ требуют значительных материальных затрат, нанося серьезный экономический ущерб, связанный как непосредственно с затратами на лечение, так и с потерей трудового времени родителей.
Таким образом, ЧБД являются проблемой, имеющей не только медицинский, но и социально-экономический аспект, что требует комплексного подхода к ее решению в реализации лечебных, реабилитационных и профилактических мероприятий для ЧБД.
Существует две основных точки зрения на причины повторных и столь частых респираторных заболеваний у ЧБД. Первая — нарушение функционирования иммунной системы, проявляющееся при неблагоприятных воздействиях внешней среды. Вторая — генетическая предрасположенность, также реализующаяся под воздействием неблагоприятных условий внешней среды. Возможно, что оба эти фактора играют роль при возникновении частой заболеваемости ОРЗ у ЧБД. Но в последние годы особое внимание исследователей уделяется состоянию иммунной системы у ЧБД.
Изучение иммунной системы ЧБД выявляет особенности ее функционирования, которые в значительной степени связаны с развитием и созреванием иммунной системы ребенка. Последние исследования показали, что у ЧБД даже в период клинического благополучия и при отсутствии признаков ОРЗ выявляются отчетливые изменения в межклеточном взаимодействии в иммунной системе: достоверно повышено содержание провоспалительных интерлейкинов (IL-2, IL-4), в том числе интерлейкинов, участвующих в хронизации воспаления (IL-6, IL-8). Это сопровождается снижением клеточной цитотоксичности, дисиммуноглобулинемией и повышением уровня клеток, экспрессирующих рецепторы, индуцирующие апоптоз. При этом индуцированная продукция провоспалительных цитокинов была недостаточной, что свидетельствует об истощении резервных возможностей иммунной системы организма ребенка. Снижение количества CD11b-клеток, куда входят гранулоциты, моноциты, натуральные киллеры и макрофаги, экспрессирующие молекулы межклеточной адгезии, а также уменьшение количества эндотелиальных клеток, экспрессирующих межклеточные молекулы адгезии 1 типа и рецепторы к риновирусам, во многом объясняет повышение чувствительности детей к повторным респираторным вирусным инфекциям и склонность их к развитию бактериальных осложнений. А недостаточность резервных возможностей интерфероногенеза, особенно в плане синтеза гамма-интерферона, осуществляющего мощную противовирусную защиту в организме, несмотря на нормальный уровень интерферона в сыворотке крови, объясняет сохранение вялотекущей реакции воспаления в организме ребенка даже при отсутствии клинических признаков ОРЗ.
Таким образом, полученные в последние годы данные свидетельствуют о том, что иммунная система ЧБД хотя и не имеет грубых первичных и приобретенных дефектов, но характеризуется крайней напряженностью процессов иммунного реагирования, нарушением межклеточной кооперации и недостаточностью резервных возможностей, что, по-видимому, является результатом длительного и массивного антигенного воздействия на организм ребенка.
Известно также, что период раннего детства характеризуется интенсивным развитием лимфоэпителиальной глоточной системы (ЛЭГС). Обычно начиная со второго года жизни ребенка постепенно формируются небные миндалины, причем у большинства детей миндалины появляются в последней четверти первого года жизни. На втором году начинается формирование глоточной миндалины (аденоидов), которая локализуется в так называемой «стратегической зоне» верхних дыхательных путей, там, где регистрируется наиболее интенсивное антигенное воздействие.
ЛЭГС обладает выраженной лимфопоэтической функцией, участвует в генерации (производстве) и «обучении» В-клонов лимфоцитов для «своего региона» — слизистой оболочки дыхательных путей, где они и осуществляют местную продукцию антител классов А и М (IgA и IgM). В небных и глоточной миндалинах имеются фолликулы с герминативными центрами, представляющими В-зону. Они относятся к тимуснезависимым структурам миндалин. Т-лимфоциты сосредоточены в экстрафолликулярной зоне миндалин и являются тимусзависимой клеточной структурой. Эпителиоциты слизистой оболочки носоглотки и миндалин образуют петлистую сеть, где сосредотачиваются мигрирующие из общего кровотока лимфоциты — так называемый лимфоэпителиальный симбиоз.
Суть лимфоэпителиального симбиоза заключается в том, что, проходя между эпителиальными клетками, лимфоциты нарушают целостность эпителиального покрова, образуя так называемые «физиологические раны» или «ходы», которые обеспечивают контакт лимфоидной ткани глотки и миндалин с внешней средой. В условиях целостности эпителиального покрова слизистой носоглотки именно эти внутриэпителиальные ходы «дозируют» поступление антигенов в ЛЭГС, обеспечивая адекватную антигенную нагрузку на лимфоидный аппарат глотки, необходимую для защиты респираторного тракта. При нарушении целостности эпителия под воздействием повторных инфекций антигенная нагрузка на ЛЭГС неизмеримо возрастает. Это может сопровождаться перенапряжением, истощением или расстройством защитных механизмов.
Функциональная активность ЛЭГС находится в тесной зависимости от возраста и морфологической зрелости ребенка. А возрастная эволюция ЛЭГС находится под генетическим контролем и зависит от морфотипа данного индивидуума. Наряду с генетически детерминированной склонностью к гиперплазии и замедленной редукции ЛЭГС на процессы ее эволюции немалое влияние оказывает воздействие внешних, фенотипических факторов. Таких факторов множество. Это — экологическое неблагополучие окружающей среды, проживание в сырых, плохо вентилируемых помещениях, большая скученность в помещениях, посещение детских коллективов, недостаточное и/или неправильное питание, неправильное лечение предшествующих респираторных заболеваний, перенесенные тяжелые заболевания, особенно инфекционные, глистная инвазия, повторяющиеся стрессовые воздействия, а также ряд других. При достаточно интенсивном воздействии фенотипических факторов они способны нарушить хрупкое равновесие между нормой и патологией, и у ребенка, имеющего генетическую предрасположенность, развивается выраженная гиперплазия ЛЭГС, нарушается лимфоэпителиальный симбиоз, создаются предпосылки для неадекватной стимуляции иммунной системы, преодоления порога ее толерантности, формирования иммунной дисфункции.
Таким образом, выявленные у ЧБД особенности клеточного и гуморального иммунитета и фагоцитоза, а также дисбаланс в цитокиновом и интерфероновом статусах свидетельствуют о напряженном функционировании иммунной системы и ЛЭГС и о возможном истощении резервов противоинфекционной резистентности у этой группы детей.
Как уже отмечалось выше, основным критерием выделения пациентов в группу ЧБД является частота заболеваемости ОРЗ. Это, однако, не исключает проведения дополнительного обследования ребенка. Прежде всего, ЧБД нуждаются в тщательном осмотре педиатром и обязательном осмотре ЛОР-врачом, включающем оценку состояния миндалин, аденоидов, придаточных полостей носа и барабанных перепонок, т. к. среди ЧБД хронические заболевания ЛОР-органов встречаются приблизительно в половине случаев.
Обязательной практикой должно быть проведение посева со слизистых зева (с миндалин) и из носа для оценки характера микробного пейзажа слизистых, т. к. микробиоценоз слизистых является одним из важнейших звеньев противоинфекционной защиты. Также может потребоваться исследование на атипичные возбудители (микоплазмоз, хламидиоз) методом ПЦР мазков со слизистой зева (определение титра антител к хламидиям и микоплазмам имеет только вспомогательное значение).
Следует учитывать, что микробиоценоз носоглотки у ЧБД нередко существенно отличается от возрастной нормы. Во-первых, как правило, инфекции респираторного тракта у этой группы детей носят смешанный вирусно-бактериальный характер, в связи с чем им многократно в течение года назначают антибактериальные препараты. Во-вторых, среди ЧБД немало детей, страдающих хроническими заболеваниями носоглотки: хроническим тонзиллитом, фарингитом, синуситом, аденоидитом и т. д., что в свою очередь влияет на микробиоценоз носо- и ротоглотки. При обследовании ЧБД можно обнаружить довольно интенсивную микробную колонизацию слизистых грибами рода Candida, стафилококками, гемофильной палочкой, в том числе гемофильной палочкой типа b, моракселлой катарралис, энтеробактериями (в том числе клебсиеллой и кишечной палочкой), микоплазмами и даже синегнойной палочкой. В носовых пазухах, лакунах небных и глоточной миндалин нередко обнаруживаются анаэробы. Выраженные нарушения микробиоценоза носоглотки снижают резистентность к патогенным возбудителям, поддерживают длительный воспалительный процесс, способствуют нарушению целостности эпителиального барьера и тем самым увеличивают антигенное воздействие и способствуют развитию хронической интоксикации.
Из методов дополнительного лабораторного и инструментального исследования целесообразно также сразу провести анализ периферической крови, общий анализ мочи и R-графию носоглотки и придаточных полостей носа в передней и боковой проекциях.
В более сложных, не поддающихся обычной терапии случаях может потребоваться консультация клинического иммунолога и/или аллерголога, а из дополнительных методов лабораторного обследования — исследование иммунограммы, в первую очередь состояния интерфероногенеза и фагоцитоза, а затем уже гуморального иммунитета, реже — клеточного иммунитета.
Медицинская помощь ЧБД складывается из трех основных направлений:
-
Восстановительные или реабилитационные мероприятия, которые направлены на снижение антигенного воздействия, санацию местных очагов хронической инфекции и повышение резистентности организма ребенка в целом. Она проводится в периоде клинического благополучия.
-
Этиопатогенетическая терапия в период ОРЗ.
-
Вакцинотерапия и неспецифическая профилактика ОРЗ.
Первое направление, восстановительное или реабилитационное лечение, хотя и является наиболее трудоемким, но оно — основа успешного ведения таких детей. Включает ряд общегигиенических мероприятий, которые необходимо проводить в семье:
-
организация рационального режима дня ребенка:
-
полноценный, достаточный по длительности сон;
-
исключение переутомления и перевозбуждения;
-
обязательные и достаточные по длительности прогулки, но без переохлаждения;
-
ограничение посещения мест большего скопления людей и т. д.;
-
полноценное питание, учитывающее возрастные особенности ребенка, склонность к аллергическим реакциям, разумное отношение к углеводистой пище и сладостям;
-
прием поливитаминных препаратов, соответствующих возрасту ребенка и его нагрузкам;
-
наконец, проведение в разумных пределах закаливающих мероприятий, таких как обливания прохладной водой, сон на свежем воздухе, ванны, души, бальнеотерапия, общий массаж, лечебная гимнастика, тренирующие занятия физкультурой.
Медикаментозная коррекция в период клинического благополучия проводится при обязательном участии ЛОР-врача, т. к. первоначально необходимо оценить объем оториноларингологической помощи. Если у ребенка хроническая ЛОР-патология и там имеется очаг хронической инфекции, то в период клинического благополучия показано наряду с общими оздоровительными мероприятиями проведение местного лечения, объем которого определяется врачами — педиатром и отоларингологом — и зависит от характера, степени выраженности и топики поражения. Местная терапия направлена на санацию хронических очагов инфекции, восстановление целостности слизистых носоглотки, подавление хронического воспаления, что, в конечном счете, обеспечивает снижение антигенной нагрузки на иммунную систему организма ребенка.
Местная терапия включает:
-
орошения слизистых солевыми растворами типа Аква Марис, Физиомер, Салин и др.;
-
использование бактерицидных пастилок типа Стрепсилс, Бронхикум, Фарингосепт и др.;
-
полоскание зева (у детей старше 4–5 лет) антисептическими растворами (Гексорал, раствор Фурацилина, отвары ромашки, зверобоя и т. д.), промывание носовых ходов, использование спрея Гексорала;
-
физиотерапевтические методы (УФО на миндалины, УВЧ, СВЧ и гелий-неоновое лазерное облучение на регионарные лимфоузлы, ингаляции с морской водой, маслом эвкалипта и т. д.);
-
в некоторых случаях аспирация содержимого лакун небных миндалин, внутрилакунарное введение антисептических паст.
Этиопатогенетическое лечение ОРЗ у ЧБД включает противовирусную терапию, противовоспалительную терапию и местную и/или системную антибактериальную терапию.
В число противовирусных лекарственных средств входят:
-
вещества, избирательно подавляющие репродукцию вирусов на различных этапах их жизненного цикла;
-
интерфероны, эндогенные низкомолекулярные белки, обладающие противовирусным, иммуномодулирующим и противоопухолевым эффектами;
-
индукторы интерферонов — высоко- и низкомолекулярные соединения природного и синтетического происхождения, стимулирующие эндогенную выработку интерферонов в организме.
В настоящее время существует более 10 групп препаратов, действие которых основано на подавлении репликации вирусов. Однако применение их в педиатрической практике резко ограничено из-за высокой токсичности, так как метаболизм размножающихся вирусов тесно связан с метаболизмом клеток человека и воздействие на вирус почти неизбежно оказывает влияние на клетки растущего и развивающегося организма ребенка. В результате в детском возрасте из противовирусных средств разрешено использование лишь единичных препаратов — Ремантадина и Альгирема.
Поэтому терапию ОРЗ следует начинать с назначения интерферонов или их индукторов. Препаратом выбора из интерферонов является комплексный препарат рекомбинантного интерферона-альфа-2b (ИНФ-альфа) с антиоксидантами — Виферон. Введенные в Виферон токоферол ацетат и аскорбиновая кислота усиливают противовирусную активность рекомбинантного ИНФ-альфа-2b в 10–14 раз, а кроме того, усиливается действие его на Т- и В-лимфоциты и нормализуется содержание IgE.
Назначают Виферон детям до 7 лет по 150 000 МЕ 2 раза в день, детям старше 7 лет по 500 000 МЕ 2 раза в день в свечах ректально в течение 5–10 дней. Затем в течение 2 недель по 2 раза в день 3 раза в неделю, затем 2 недели по 2 свечи 2 раза в неделю, затем по 1 свече 1 раз в день 2 раза в неделю, далее по 1 свече 1 раз в неделю 2 недели. Одновременно в остром периоде можно назначить местное лечение мазью Виферона — обработка ротоглотки и интраназальное использование 2–4 раз в день.
При вирусной инфекции у детей старше 2,5 лет также используется индуктор интерфероногенеза Арбидол. Арбидол детский назначается по 1 таблетке 2 раза в день в первые 2 дня заболевания, затем по 1 таблетке 2 раза в день 1 раз в 3 дня 3–5 раз. Детям старше 6 лет возможно назначение другого индуктора интерфероногенеза Амиксина.
При гриппе применяют вещества, подавляющие репликацию вирусов, римантадин (Ремантадин, Альгирем) и амантадин. Они препятствуют адсорбции вирусов, проникновению в клетку хозяина и «раздеванию» вируса. Римантадин и амантадин обладают активностью в основном по отношению к вирусу гриппа А. Поэтому показанием к их назначению является установленная или высоковероятная гриппозная этиология болезни (соответствующая эпидемическая обстановка, «запаздывание» катаральных симптомов ОРЗ на период от нескольких часов до 1–2 дней, тяжелая, прогрессирующая симптоматика ОРЗ), поскольку в этой ситуации высок риск неблагоприятного исхода заболевания.
Ремантадин назначают детям старше 1 года внутрь из расчета 5 мг/кг массы тела в сутки (но не более 15 мг) в 2 приема в течение 5 дней. Доза Альгирема в 1 день лечения составляет 10 мг 3 раза, во 2 и 3 дни — 10 мг 2 раза, на 4 день — 10 мг 1 раз в сутки.
Противовоспалительной терапией является фенспирид (Эреспал). Действие Эреспала основано на том, что, нарушая транспорт ионов кальция в клетки, препарат снижает активность фосфолипазы А2. Это, в свою очередь, замедляет скорость каскада реакций метаболизма арахидоновой кислоты. В результате замедляется образование простагландинов, лейкотриенов и тромбоксанов — основных факторов, инициирующих сосудистую фазу воспаления, уменьшается степень воспалительного отека тканей и секреторной активности бокаловидных клеток слизистых оболочек. Кроме того, Эреспал подавляет синтез гистамина и уровень экспрессии альфа1-адренорецепторов. Это способствует меньшей напряженности 2-й фазы воспаления — фазы клеточной инфильтрации. За счет влияния на все фазы воспаления, Эреспал уменьшает отек, гиперпродукцию слизи, способствуя этим восстановлению активности реснитчатого эпителия и дренажной функции респираторного тракта. Эреспал оказывает положительное влияние на функциональное состояние бронхов. Отсутствие возрастных ограничений и высокий терапевтический эффект позволяет рассматривать Эреспал в качестве препарата выбора противовоспалительной терапии острых инфекций респираторного тракта у детей. Эреспал назначается в дозе 4 мг/кг массы тела (до 10 кг 2–4 чайной ложки, после 10 кг 2–4 ст. л.) в сутки в течение 5–7 дней.
Особое значение имеет проведение местного антибактериального лечения. Местная антибактериальная терапия была предложена сравнительно недавно, но уже привлекла к себе пристальное внимание ЛОР-врачей и педиатров, так как она позволяет значительно снизить частоту использования системной антибактериальной терапии, способствует санации хронических очагов инфекции и тем самым значительно уменьшает антигенную нагрузку на ЛЭГС.
Препаратом местной антибактериальной терапии является фюзафюнжин — Биопарокс. Причем фюзафюнжин относится к антибиотикам растительного происхождения. Биопарокс используется в виде спрея для орошения слизистой. Орошения проводят 4 раза в день. При этом создается достаточно высокая концентрация препарата в месте введения. Так, при использовании Биопарокса в тканях носоглотки достигается концентрация растительного антибиотика фюзафюнжина от 160 до 240 мкг/л, что вполне достаточно для подавления инфекционного процесса. Ограничением использования этого препарата в детском возрасте является возраст. В частности, препараты назначают детям только старше 2,5 лет. Важно, что наряду с антибактериальным действием Биопарокс обладает противовоспалительным эффектом. Он снижает продукцию свободных радикалов кислорода, подавляя синтез молекул межклеточной адгезии 1 типа, способствует снижению продукции и высвобождению провоспалительных медиаторов и выбросу ранних интерлейкинов воспаления, оказывая отчетливое регулирующее влияние на местную воспалительную реакцию.
Поскольку приблизительно 70% острых респираторных инфекций имеет вирусную природу, они не требуют проведения системной антибактериальной терапии. Это положение касается как большинства заболеваний верхних отделов респираторного тракта, так и острых бронхитов и трахеобронхитов. Многочисленные исследования показали, что назначение системных антибиотиков при респираторной вирусной инфекции не приводило к сокращению сроков лечения и числа осложнений.
Показанием к назначению системных антибиотиков является развитие явно бактериального воспалительного процесса в дыхательных путях: гнойного среднего отита, гнойного синусита, ангины, ларингита с явлениями стеноза гортани 2–3-й степени, острого гнойного трахеобронхита/бронхита, пневмонии, а также признаки микоплазменной или хламидийной этиологии ОРЗ. Поэтому необходимо знать критерии бактериального воспаления. На бактериальную природу респираторной инфекции указывают:
-
длительная (более 3 дней), фебрильная (выше 38,5 °С) температура;
-
появление гнойных наложений, гнойного или слизисто-гнойного отделяемого;
-
выраженная интоксикация;
-
при отсутствии лихорадки и выраженной интоксикации — затяжной характер респираторной инфекции (более двух недель), основным проявлением которой является упорный непродуктивный кашель (признаки возможной хламидийной или микоплазменной инфекции).
Совокупность этих признаков может свидетельствовать в пользу бактериальной природы или присоединения бактериального компонента воспаления, что требует назначения системной антибактериальной терапии.
Наряду с этим прямым показанием к назначению системных антибактериальных средств являются:
-
предположение или установленный диагноз пневмонии;
-
эпиглоттит;
-
гнойный отит;
-
гнойный синусит;
-
острый стрептококковый тонзиллит (фарингит);
-
паратонзиллярный абсцесс.
Необоснованное назначение системных антибиотиков приводит к повышению риска побочных явлений, нарушению микробного биоценоза и способствует распространению лекарственной устойчивости.
Кроме того, при лечении ОРЗ проводится симптоматическая терапия, к которой относятся жаропонижающие и противокашлевые препараты, назальные деконгестанты.
Вакцинация ЧБД и проведение неспецифической профилактики ОРЗ
Прежде всего, хотелось бы отметить, что частые ОРЗ у ребенка не являются противопоказанием к проведению прививок, поскольку ОРЗ не относятся к тем заболеваниям, течение которых может утяжеляться в результате вакцинации. Кроме того, ОРЗ не повышают риск развития прививочных реакций и осложнений. Таким образом, указание на частые респираторные инфекции у ребенка не должно являться поводом для отвода от прививок. В тех случаях, когда очередной эпизод респираторной инфекции совпадает с декретируемым сроком плановой календарной прививки, требуется перенести вакцинацию на более позднее время.
В осенний период времени года с профилактической целью используют бактериальный иммунокорректор Рибомунил, бактериальный иммунокорректор Бронхо-мунал, топический бактериальный иммунокорректор Имудон, топический бактериальный иммунокорректор ИРС 19. Все они назначаются за 2–3 месяца до начала эпидемии ОРЗ, т. е. в конце сентября — октябре-ноябре.
Рибомунил назначают вне зависимости от возраста, детям старше 6 месяцев, по 1 дозе утром, натощак. В первый месяц лечения Рибомунил принимают ежедневно 4 дня в неделю в течение 3 недель. В последующие 5 месяцев в первые 4 дня каждого месяца. Бронхо-мунал назначают детям от 6 месяцев до 12 лет по 3,5 мг, детям старше 12 лет 7 мг утром, натощак, 1 раз в день в течение 10 дней, затем через 20-дневный интервал еще 2 раза по 10 дней. Имудон назначается детям старше 3 лет по 1 таблетке для рассасывания 4 раза в день, курсом 20 дней. ИРС 19, суспензия для интраназального введения в виде спрея, назначается детям старше 3 лет по 1 дозе в каждый носовой ход 2 раза в день курсом от 14 до 30 дней.
Необходимо помнить, что все эти иммунокорректоры дают побочные реакции со стороны пищеварительной системы и аллергические реакции.
Можно также назначать гомеопатические препараты. Например, Оциллококцинум назначают по 1 дозе (1 тубу растворить в 1/2 стакана воды) 1 раз в неделю детям всех возрастов курсом до 3 месяцев. Анаферон детский — детям с 6 месяцев назначают по 1 таблетке в день сублингвально, курсом до 3 месяцев. Афлубин — по 5 капель детям с 6 месяцев до 12 лет, детям старше 12 лет по 10 капель, растворить в 15 мл воды 2 раза в день курсом 3 месяца. Инфлюцид назначают детям старше 6 лет по 1 таблетке сублингвально 2 раза в день курсом 1 месяц.
Гомеопатические препараты практически не имеют побочных действия, редко отмечаются аллергические реакции, и их можно назначать в эпидемический период времени.
Частая респираторная заболеваемость — одно из основных показаний к вакцинации детей против гриппа. Как показали исследования последних лет, прививки против гриппа не только снижают заболеваемость данной инфекцией, но и сокращают частоту вирусной ОРЗ другой этиологии. Объяснений этому феномену несколько. Гриппозные вакцины являются сильными индукторами интерфероногенеза, поэтому их введение приводит не только к формированию специфической иммунной защиты против гриппа, но и может способствовать неспецифической профилактике других ОРЗ за счет повышения уровня интерферона. Играет роль и поликлональная активация иммунной системы: заражение тем или иным респираторным патогеном способно вызывать не только специфический иммунный ответ, но и активировать механизмы иммунологической памяти в отношении других возбудителей, с которыми организм больного встречался ранее. Вероятно, все вышеизложенное и объясняет тот факт, что иммунизация детей от гриппа сопровождается не только снижением частоты самого гриппа, но и других вирусных ОРЗ.
Для иммунизации ЧБД предпочтительнее использовать современные инактивированные гриппозные сплит- или субъединичные вакцины. Наиболее эффективна вакцинация в тех случаях, если она проводится планово — в осенние месяцы, еще до подъема заболеваемости респираторными инфекциями. Дети в возрасте от 6 месяцев и до 9 лет, ранее не болевшие гриппом, вакцинируются двукратно с интервалом в 4 недели, а дети, иммунизированные в предшествующие годы, болевшие гриппом и дети старше 9 лет — прививаются однократно. Разовая доза инактивированных гриппозных сплит- и субъединичных вакцин составляет 0,25 мл — для детей в возрасте от 6 месяцев до 3 лет и 0,5 мл — для детей в возрасте 3 лет и старше.
Особо следует подчеркнуть, что активная специфическая иммунизация против гриппа, проведенная у ЧБД на фоне применения бактериальных иммунокорректоров, существенно повышает эффективность вакцинации.
По вопросам литературы обращайтесь в редакцию.
Г. А. Самсыгина, доктор медицинских наук, профессор Г. С. Коваль, кандидат медицинских наук РГМУ, Москва
