Лечащий Врач #3, 2009
Фотодинамическая терапия в лечении гинекологических заболеваний
Поиск новых высокотехнологичных методов лечения в гинекологии обусловлен: неудовлетворительными результатами лечения существующими методами; увеличением в структуре заболеваемости удельной доли пациенток с тяжелой экстрагенитальной патологией, ограничивающей использование того или иного метода лечения, применение анестезиологического пособия или длительного приема лекарственных препаратов определенных групп; созданием новых минимально инвазивных, органосохраняющих методов лечения, а кроме того, возможностью их амбулаторного использования.
Одним из таких перспективных и высокотехнологичных методов является фотодинамическая терапия (ФДТ), основанная на селективной деструкции пролиферирующих клеток в результате фотохимического воздействия при взаимодействии накапливающегося в них фотосенсибилизатора (ФС) и активирующего его света определенной длины волны [9, 14].
На протяжении более чем 40-летней истории существования метода ФДТ его развитие шло как по пути поиска «идеального» ФС (с высокой аффинностью и селективностью накопления в патологических клетках, стремительной фармакодинамикой и низкой кожной фототоксичностью), так и по пути создания мощных источников света и совершенствования световолоконной оптики для доставки излучения к тканям [4].
Суммируя итоги многолетнего использования ФДТ в медицине, можно констатировать, что в начале своего использования ФДТ была предназначена либо для лечения ранних форм злокачественных новообразований, либо служила компонентом комбинированной паллиативной терапии рака различных локализаций [8, 11]. Однако в настоящее время ФДТ признана не только стандартным методом терапии злокачественных опухолей, но и значительно расширился спектр заболеваний неопухолевой природы, для лечения которых также с успехом применяется ФДТ [6, 10].
Ее применение в гинекологии началось с использования в лечении злокачественных поражений шейки матки и вульвы [1, 5, 7, 12].
Однако оценка роли и места ФДТ, а также ее эффективность при лечении таких нозологических форм, как фоновые и предраковые заболевания шейки матки и эндометрия, склеротический лишай и плоскоклеточная гиперплазия вульвы, изучены недостаточно.
Анализ современного состояния проблемы позволяет признать, что применение ФДТ в гинекологии является одним из перспективных направлений. Это обусловливает необходимость проведения дальнейших клинических исследований.
Материалы и методы
Эффективность ФДТ изучалась при таких нозологических формах гинекологических заболеваний, как неопухолевые заболевания шейки матки, гиперплазия эндометрия и дистрофические процессы слизистой вульвы.
Первую группу больных составили 72 женщины с фоновыми и предраковыми заболеваниями шейки матки в возрасте от 19 до 67 лет (средний возраст 43,2 ± 0,3 года) По нозологическим формам все больные распределились следующим образом: у 37 (51,38%) пациенток диагностирована эктопия шейки матки, у 14 (19,4%) — лейкоплакия, у 7 (9,72%) — эндометриоз, у 9 (12,5%) — дисплазия шейки матки (CIS I–II) и у 5 (6,9%) пациенток эктропион на фоне незначительной рубцовой деформации шейки матки. Группу сравнения составили 30 женщин в возрасте от 28 до 67 лет (средний возраст 45,2 ± 0,2 года). Из них 13 (43,3%) пациенток с эктопией, причем у 6 — эктопия сочеталась с гипертрофией шейки матки; 6 (20%) пациенток с лейкоплакией, из которых у 5 лейкоплакия сочеталась с гипертрофией шейки матки, у 11 (36,6%) больных — эктропион на фоне рубцовой деформации шейки матки. Исходя из требований доказательной медицины и для получения истинного представления о характере патологического процесса в шейке матки, нами было проведено комплексное клиническое обследование, включающее микробиологические, кольпоскопические, цитологические и гистологические методы.
В качестве предоперационной подготовки всем женщинам с обнаруженной инфекцией половых путей проводилась этиотропная и иммуномодулирующая терапия с последующим назначением эубиотиков для нормализации микробиоценоза влагалища.
Лазерное воздействие на шейку матки осуществлялось в первую фазу менструального цикла через 2 часа после местной аппликации на экзоцервикс ФС Фотодитазин в виде 0,5% геля или внутривенного введения ФС Фотодитазин в дозе 0,5 мг/кг веса. Облучение шейки матки осуществлялось с помощью диодного лазерного аппарата «Аткус-2» («Полупроводниковые приборы», Россия). Длина волны излучения — 662 нм, плотность энергии 80–250 Дж/см2, время воздействия от 8 до 20 минут.
В качестве метода сравнения у больных с заболеваниями шейки матки применялось рутинное диатермохирургическое (ДХ) лечение (диатермокоагуляция и диатермоконизация) с помощью аппарата «ЭС 500 М».
Вторую группу больных составили 92 пациентки с морфологически верифицированным диагнозом гиперпластического процесса эндометрия (ГПЭ). Из них фотодинамическая деструкция эндометрия была выполнена у 60 больных, находящихся в пери- и постменопаузальном периоде, в возрасте 41–68 лет (средний возраст 50,8 ± 1,5 года). По характеру выявленной патологии эндометрия в группе ФДТ больные распределились следующим образом: 2 пациентки — гиперплазия с атипией эндометрия, 10 больных простой и 24 больных сложной гиперплазией без атипии эндометрия, у 24 пациенток выявлены полипы эндометрия. Все пациентки этой группы имели сопутствующую экстрагенитальную патологию различной степени выраженности, послужившую основанием для выбора в качестве метода лечения ФДТ, причем в 85% случаев отмечалось сочетание различных нозологических форм. Так, более чем у половины больных (56,5%) преобладало нарушение жирового обмена, гипертоническая болезнь у 55%, варикозная болезнь вен нижних конечностей у 51,6%, ишемическая болезнь сердца у 10%, хронический бронхит, желчекаменная болезнь, хронический панкреатит встречались у 8,3% пациенток, хронический тонзиллит и нейроциркуляторная астения у 7% больных; жировой гепатоз, мочекаменная болезнь у 5%, хронический гастрит, узловой зоб, сахарный диабет 2-го типа и хронический пиелонефрит у 3,3% больных.
В контрольную группу были включены 32 женщины в возрасте 46–53 лет (средний возраст 52 ± 1,4 года), получившие гормональную терапию. У пациенток этой группы не было выявлено тяжелой сопутствующей патологии. Так, наиболее часто у них встречались нарушение жирового обмена (у 5 (15,6%) женщин) и нейроциркуляторная астения (у 4 (21,5%) больных).
Предоперационное обследование пациенток с ГПЭ было стандартно и включало ультразвуковое исследование органов малого таза, гистероскопию с тотальным кюретажем эндометрия и последующим гистологическим исследованием полученного материала, а также обследование шейки матки.
С целью выбора наиболее оптимальных временных параметров начала облучения, соответствующего максимуму накопления ФС в эндометрии, in vivo использован метод локальной флуоресцентной спектроскопии с помощью спектрально-флуоресцентной диагностической установки «Спектр-Кластер» («Кластер», ИОФРАН, Россия). Для флуоресцентного детектирования эндометрия применяли лазерное излучение с длиной волны 632,8 нм, что позволило селективно возбуждать флуоресценцию ФС без генерации флуоресценции эндогенных флуорохромов тканей. Измерения проводились до введения ФС (оценка эндогенной аутофлуоресценции) и через 30, 60, 90, 120 и 160 минут после внутривенного введения ФС (экзогенная возбужденная флуоресценция тканей).
В ходе спектрально-флуоресцентных исследований было определено, что если до введения ФС эндогенная флуоресценция эндометрия ничтожно мала, то после введения ФС во всех точках измерения экзогенная флуоресценция эндометрия достоверно выше, а регистрируемый спектр фактически представлял собой спектр флуоресценции введенного препарата Фотодитазин в диапазоне 650–750 нм. Мощность лазерного излучения на торце волоконно-оптического катетера (световода) составляла 5 мВт, время экспозиции — 60 мс. Максимальные значения флуоресценции, а следовательно, и накопления Фотодитазина регистрировались в эндометрии через 1,5–2 часа после внутривенного введения. Именно эти исследования и явились определяющими в оптимизации времени начала лазерного облучения полости матки.
Согласно методике, сеанс облучения слизистой матки осуществлялся на аппарате «Аткус-2» (длина волны 662 нм, мощность на выходе 1,85–2,0 Вт) через 1,5–2 часа после внутриматочного и/или внутривенного введения ФС Фотодитазин в дозе 1–1,5 мг/кг без применения анестезиологического пособия. Нами использован световод с оригинальным оптическим внутриматочным баллонным диффузором («Полироник», Россия). Расширения цервикального канала не требовалось, что было обусловлено небольшим диаметром (3 мм) баллонного световода, проводимого через цервикальный канал. После введения в полость матки баллон заполняли стерильным раствором дистиллированной воды в количестве 3,5 мл для принятия им треугольной формы, соответствующей анатомической форме полости матки, и с целью равномерного распределения лазерного излучения. Световое воздействие проводили в непрерывном или фракционном режиме, длительность облучения составила 15–40 минут, при плотности энергии 150–300 Дж/см2.
Для лечения пациенток контрольной группы у 17 больных применялись агонисты гонадотропин-релизинг-гормона, гестагены использованы у 13 больных и антиэстрогены получали 2 пациентки. Длительность гормонотерапии составляла 3–6 месяцев.
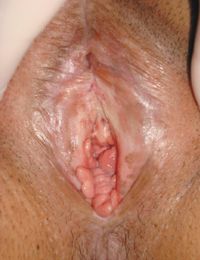
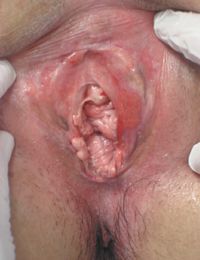
Третью группу больных составили пациентки с дистрофическими заболеваниями вульвы. Эффективность ФДТ была изучена при лечении 6 пациенток с доброкачественными заболеваниями вульвы (средний возраст 54,2 ± 0,5 года). Из них 4 больных со склеротическим лишаем вульвы и 2 — с плоскоклеточной гиперплазией вульвы. Для уточнения характера выявленной патологии производилось онкоцитологическое исследование соскоба с вульвы, вульвоскопия, ПЦР-диагностика для выявления вируса папилломы человека различных типов, а на заключительном этапе диагностики была проведена биопсия патологических участков.
ФДТ была проведена с использованием ФС Фотодитазин в комбинации внутривенного введения в дозе 1 мг/кг и местной аппликации на патологический очаг вульвы 1 мл 0,5% геля-пенетратора Фотодитазин. Время экспозиции лазерного облучения полупроводниковым лазером «Аткус-2» под местной анестезией 2% раствора лидокаина составило 10–30 минут при плотности световой дозы 100–200 Дж/см2.
Результаты исследования
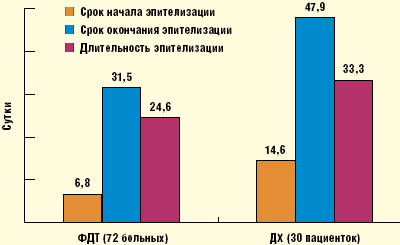
В первой группе больных при наблюдении за репаративными процессами шейки матки после ФДТ было отмечено формирование тонкого струпа в зоне облучения через 24 часа после процедуры. Начало краевой эпителизации наблюдалось на 5–8 сутки при отсутствии лейкоцитарной инфильтрации (рис. 1, 2). Полная эпителизация выявлена при этом через 4–8 недель (31,5 ± 0,7 дня) (рис. 3), тогда как в группе ДХ-лечения средний срок завершения эпителизации составил 47,9 ± 0,9 дня (р < 0,001) (рис. 4). Побочные эффекты при применении ФДТ наблюдались у 8 (11,1%) больных и заключались лишь в неполной эпителизации шейки матки. И, напротив, у больных, подвергшихся ДХ-воздействию, отмечалась достоверно более высокая частота и разнообразие послеоперационных осложнений. Так, 76,6% пациенток беспокоили боли в нижних отделах живота, у 6,7% отмечены кровотечения в послеоперационном периоде, у 6,7% — обострение хронического сальпингоофорита, у 30% — кольпит, у 20% — неполная эпителизация шейки матки. Изучение отдаленных результатов после ДХ-лечения (через 6–9 месяцев) выявило, что болевой синдром беспокоил 13,3% пациенток, рубцовая деформация и «синдром коагулированной шейки» выявлен у 43,3%, «наботовы» кисты у 33,3% и эндометриоидные гетеротопии у 13,3% больных. Эти данные сопоставимы с литературными, в которых осложнения после ДХ-метода лечения отмечены в 6,2–40% случаев [2].
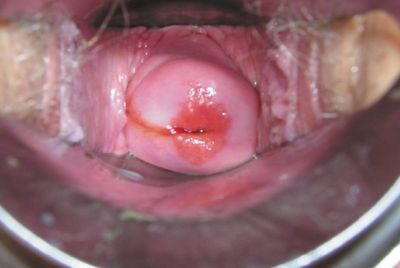
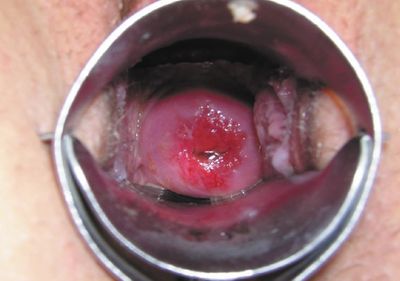
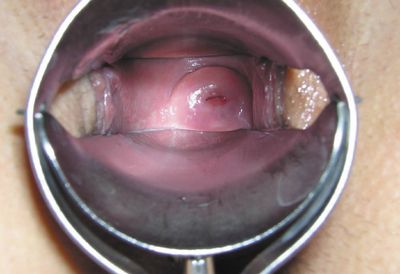
ФДТ при лечении фоновых и предраковых заболеваний шейки матки считалась эффективной при наступлении полной клинической ремиссии. По данным кольпоскопии и цитологического исследования частота полной клинической ремиссии после ФДТ у больных первой группы составила по нашим наблюдениям 88,9%.
У больных второй группы с ГПЭ эффективность ФДТ проводилась на основании данных ультразвукового исследования срединных маточных структур на 7 и 30 сутки после процедуры, а также спустя 3, 6 и 12 месяцев после операции. Анализ полученных данных показал, что у всех пациенток на 7 день после проведения сеанса ФДТ отмечалось незначительное расширение полости матки (М-эхо варьировало от 4 до 7 мм), что связано со скоплением в полости незначительного количества жидкости. Однако на 30 сутки во всех наблюдениях отмечено линейное М-эхо. Через 6 месяцев в 88,7% случаев М-эхо составило от 2 до 4 мм. У 2 пациенток имел место рецидив ГПЭ в сроки от 2 до 6 месяцев, что потребовало проведения повторной процедуры ФДТ.
У 20 пациенток прослежены отдаленные результаты лечения в сроки до 12 месяцев. У всех из них наблюдалась стойкая аменорея на фоне линейного М-эхо по данным ультразвукового исследования срединных маточных структур. Однако у одной пациентки сохранилась менструальная функция при отсутствии патологии эндометрия по данным морфологического исследования соскоба из полости матки.
Диагностическая гистероскопия выполнялась через 12 месяцев после проведения процедуры у всех пациенток с атипической гиперплазией эндометрия и у 18 больных с ГПЭ, получавших лечение методом ФДТ. Гистероскопическая картина была представлена атрофией эндометрия на фоне отсутствия облитерации полости матки.
Побочные эффекты были отмечены в 15 наблюдениях и заключались в слабо и умеренно выраженном болевом синдроме во время и непосредственно после проведения сеанса ФДТ, что быстро купировалось назначением ненаркотических анальгетиков в течение 12 часов после операции. В 3 случаях имело место повышение температуры до субфебрильных цифр на вторые сутки после операции, что потребовало назначения профилактической антибактериальной терапии. В одном случае на 10 день после проведения ФДТ у пациентки с варикозной болезнью был диагностирован тромбоз в бассейне большой подкожной вены бедра. Больная была прооперирована в плановом порядке.
Оценка эффективности гормональной терапии проводилась через 6 месяцев и основывалась на данных аспирационной биопсии эндометрия. Клиническая ремиссия отмечена в 84,4%. При этом у 5 больных (15%) с сочетанной и соматической патологией возник рецидив ГПЭ в сроки от 6 до 24 месяцев после окончания лечения. Среди побочных эффектов преобладали прибавка массы тела и мастодиния, при этом максимальное количество побочных реакций отмечалось в группе пациенток, получающих агонисты гонадотропин-релизинг-гормона.
У больных 3 группы лечебный эффект оценивался визуально и на основании указаний на наличие или отсутствие зуда в области вульвы. Так, исчезновение зуда в области вульвы отмечено у трех из четырех больных склеротическим лишаем вульвы. У всех больных плоскоклеточной гиперплазией было проведено цитологическое исследование соскоба с вульвы и вульвоскопия, на основании которых было достоверно диагностировано клиническое излечение. При наблюдении через 3 месяца лечебный эффект сохранялся. У одной больной склеротическим лишаем вульвы потребовалось проведение повторного сеанса ФДТ ввиду сохраняющихся клинических симптомов заболевания, после чего был достигнут положительный лечебный эффект. Больная прослежена в течение 3 месяцев после процедуры. Побочные реакции были отмечены во всех случаях и заключались в слабо, умеренно и сильно выраженном болевом синдроме во время проведения процедуры ФДТ, что ограничивало подведение адекватной терапевтической дозы световой энергии и потребовало досрочного завершения сеанса облучения у одной пациентки.
Обсуждение
Анализ результатов проведения ФДТ с использованием в качестве ФС Фотодитазина при лечении фоновых и предопухолевых заболеваний шейки матки показал, что время наступления и скорость репаративных процессов в слизистой шейки матки в группе женщин, подвергшихся ФДТ, существенно отличалось от аналогичных показателей у пациенток, которым проведено ДХ-лечение. Сроки полной эпителизации экзоцервикса у больных первой группы были в 1,5 раза короче, чем в группе сравнения. При этом число осложнений оказалось в 7 раз меньше, чем при использовании диатермокоагуляции. Таким образом, сравнительная характеристика результатов лечения ДХ-методом и ФДТ указывает на ряд преимуществ последней: более короткие сроки эпителизации шейки матки и меньшая частота осложнений в послеоперационном периоде. Кроме того, ФДТ позволяет селективно воздействовать на патологический очаг за счет избирательного накопления ФС в патологической ткани и локального подведения света. Нельзя не отметить также тот факт, что метод фотодеструкции, ввиду своей деликатности, позволяет сохранить анатомическую и функциональную целостность шейки матки, что трудно переоценить при лечении нерожавших пациенток репродуктивного возраста.
Мониторинг отдаленных результатов в группе пациенток с гиперплазией эндометрия показал, что ФДТ была эффективна в 87% случаев, а в случаях рецидива было возможно повторное проведение сеанса ФДТ с достижением полной клинической ремиссии. В отличие от пациенток, получавших гормональную терапию в течение 6 месяцев, у этих больных не отмечено сколько-нибудь серьезных осложнений и побочных эффектов. В то же время в группе сравнения наиболее часто наблюдались такие нежелательные побочные эффекты, как увеличение веса у 29 больных и мастодиния у 13 пациенток. Причем эти проявления носили стойкий характер. В 15% случаев имел место рецидив заболевания, тогда как у женщин после ФДТ рецидив заболевания, купированный повторным сеансом фотодеструкции, отмечен только у 2 пациенток (3%).
Таким образом, фотодинамическая деструкция эндометрия обладает рядом преимуществ в сравнении с гормональной терапией, в частности, позволяет высокоселективно удалять функциональный и базальный слой слизистой оболочки матки, не приводя впоследствии к облитерации полости матки. Кроме этого методика проведения процедуры не требует применения анестезиологического пособия, что делает возможным ее использование в амбулаторных условиях, что особенно важно у пациенток, отягощенных различной экстрагенитальной патологией, являющейся противопоказанием к гормональному или хирургическому лечению.
Не менее удовлетворительные результаты получены при использовании ФДТ при лечении дистрофических изменений вульвы. Полная клиническая ремиссия отмечена у 5 из 6 больных (рис. 5, 6). Одной пациентке со склеротическим лишаем вульвы потребовалось проведение повторного сеанса ФДТ, после чего было диагностировано клиническое излечение. Во всех случаях был зафиксирован хороший косметический эффект, что особенно актуально для молодых пациенток репродуктивного возраста.
Таким образом, полученные результаты клинической апробации метода фотодинамической терапии с использованием ФС Фотодитазин при лечении женщин с патологией шейки матки, эндометрия и вульвы неопухолевого генеза показали его высокую лечебную активность, минимальное количество осложнений и побочных эффектов. Метод отличается избирательностью, а также деликатным характером воздействия на патологические ткани. Кроме того, простота выполнения процедуры ФДТ, а также отсутствие необходимости в анестезиологическом пособии делают возможным использование его в амбулаторных условиях, что обусловливает необходимость внедрения его в широкую клиническую практику.
Литература
- Дадвани С. А., Зуев В. М., Харнас С. С. и др. Фотодинамическая терапия в гинекологии // Лазерная медицина. 2000. Т. 4, вып. 4, с. 72–79.
- Заболевания шейки матки, влагалища и вульвы (Клинические лекции) / Под ред. проф. В. Н. Прилепской. М.: МЕДпресс, 2000, с. 432.
- Зангиева Ф. А. Лазерная флюоресцентная диагностика и фотодинамическая терапия рака вульвы, дисс. кан. мед. наук, 2005.
- Странадко Е. Ф. Исторический очерк развития фотодинамической терапии // Лазерная медицина. 2002. Т. 6, № 6, с. 4–8.
- Чулкова О. В., Новикова Е. Г., Соколов В. В., Чулкова Е. А. Диагностика и лечение фоновых и предраковых заболеваний вульвы // Практическая онкология. 2006. Т. 7. № 4, с. 197–204.
- Akaza E., Mori R., Yuzawa M. Long-term results of photodynamic therapy of polypoidal choroidal vasculopathy // Retina. 2008, May; 28 (5): 717–22.
- Ascencio M., Collinet P., Cosson M., Vinatier D., Mordon S. The place of photodynamic therapy in gynecology // Gynecol Obstet Fertil. 2007, Nov; 35 (11): 1155–1165. Epub 2007, Oct 22.
- Juarranz A., Jaen P., Sanz-Rodriguez F., Cuevas J., Gonzalez S. Photodynamic therapy of cancer. Basic principles and applications // Clin Transl Oncol. 2008, Mar; 10 (3): 148–154.
- McCaughan J. S. Jr. Photodynamic therapy: a review // Drugs Aging. 1999, Jul; 15 (1): 49–68.
- MacCormack M. A. Photodynamic therapy in dermatology: an update on applications and outcomes // Semin Cutan Med Surg. 2008, Mar; 27 (1): 52–62.
- Sibata C. H., Colussi V. C., Oleinick N. L., Kinsella T. J. Photodynamic therapy in oncology // Expert Opin Pharmacother. 2001, Jun; 2 (6): 917–927.
- Yamaguchi S., Tsuda H., Takemori M., Nakata S., Nishimura S., Kawamura N., Hanioka K., Inoue T., Nishimura R. Photodynamic therapy for cervical intraepithelial neoplasia // Oncology. 2005; 69 (2): 110–116. Epub 2005, Aug 23.
- Waksman R., Leitch I. M., Roessler J., Yazdi H., Seabron R., Tio F., Scott R. W., Grove R. I., Rychnovsky S., Robinson B., Pakala R., Cheneau E. Intracoronary photodynamic therapy reduces neointimal growth without suppressing re-endothelialisation in a porcine model // Heart. 2006, Aug; 92 (8): 1138–1144. Epub 2006, Jan 6.
- Wilson B. C., Patterson M. S. The physics, biophysics and technology of photodynamic therapy // Phys Med Biol. 2008, May 7; 53 (9): R61–109. Epub 2008, Apr 9.
О. В. Макаров, доктор медицинских наук, профессор
А. З. Хашукоева, доктор медицинских наук, профессор
О. Б. Отдельнова
С. А. Рехвиашвили, кандидат медицинских наук
Л. И. Залевская
РГМУ, Москва
